
分析 ①导致雾霾形成的主要污染物是pM2.5;空气污染指数指空气被污染的程度,以二氧化硫、二氧化氮和可吸入颗粒物等污染物的浓度计算;
②浓氨水和二氧化碳反应生成碳酸氢铵,碳酸氢钠的溶解度很小,以晶体形式析出,碳酸氢铵和氯化钠两者交换成分进反应;根据化合物中元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%,进行分析解答;
③重金属离子能与氢氧根离子结合成碱,地沟油的主要成分是高级脂肪酸甘油酯.
解答 解:①PM2.5”是指大气层中直径≥2.5μm的颗粒物,能被肺吸收并进入血液,对人体危害很大,是形成雾霾的主要污染物;空气质量的高低与空气中所含污染物的数量有关,可以用二氧化硫、二氧化氮和可吸入颗粒物等污染物污染指数来表示;指数越大,级别越高,说明污染越严重,
故答案为:PM2.5;NO2;
②浓氨水和二氧化碳反应生成碳酸氢铵,NH3•H2O+CO2=NH4HCO3,碳酸氢铵和氯化钠反应生成碳酸氢钠和氯化铵NH4HCO3+NaCl=NH4Cl+NaHCO3↓,总反应为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl,CaSO4•2H2O中,硫元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%=$\frac{32}{172}$×100%,(NH4)2SO4中,硫元素的质量分数=$\frac{相对原子质量×原子个数}{相对分子质量}$×100%=$\frac{32}{132}$×100%,硫元素的质量分数较高的是,(NH4)2SO4,
故答案为:NaCl+NH3+CO2+H2O=NaHCO3↓+NH4Cl;(NH4)2SO4;
③工业废水中的重金属离子与加入的碱反应生成难溶性的含重金属离子的氢氧化物;地沟油的主要成分是高级脂肪酸甘油酯,水解生成高级脂肪酸和甘油,
故答案为:氢氧化物;水解.
点评 本题考查环境污染及治理有关知识,为常见题型和高频考点,有利于培养学生的良好科学素养,题目难度不大,注意相关基础知识的积累.


科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
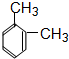 ; ②
; ②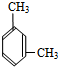 ; ③
; ③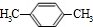 ; ④
; ④ .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Cu2+ | B. | Al3+ | C. | CH3COO- | D. | HCO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用丁达尔效应鉴别Fe(NO3)3溶液和Fe2(SO4)3溶液 | |
| B. | 用加热、称重的方法鉴别Na2CO3固体和NaHCO3固体 | |
| C. | 将某气体通入品红溶液中,溶液褪色,说明该气体一定是SO2 | |
| D. | 用铂丝蘸取溶液在酒精灯火焰上灼烧,若火焰呈黄色,则溶液中一定含有K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 纤维素、蛋白质、油脂都是天然有机高分子化合物 | |
| B. | 燃煤中加入CaO后可减少酸雨的发生气体的排放 | |
| C. | 纤维素在人体内可水解为葡萄糖,是人类重要的营养物质之一 | |
| D. | 明矾是一种水处理剂,可用于水的杀菌、消毒 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | H2O2 | B. | CaLiH3 | C. | NaN3 | D. | H2SO4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .
. .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com