
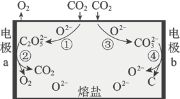
【题目】为减少二氧化碳排放,我国科学家设计熔盐电解池捕获二氧化碳的装置,如下图所示。下列说法不正确的是
A.CO2过量排放是导致温室效应的原因之一
B.过程②中C2O52-在a极上发生了还原反应
C.过程③中的反应可表示为:CO2+O2-=CO32-
D.CO2最终转化为C和O2
【答案】B
【解析】
由装置图可知,a极上,电极反应有:4CO2+2O2-=2C2O52-,2C2O52--4e-=4CO2↑+O2↑,总的电极反应为:2O2--4e-=O2↑;b极上,电极反应有:CO2+O2-=CO32-,CO32-+4e-=C+3O2-,总的电极反应为:CO2+4e-=C+2O2-;熔盐电解池的总的化学方程式为:CO2![]() C+O2,据此分析解答。
C+O2,据此分析解答。
A.太阳短波辐射可以透过大气射入地面,而地面增暖后放出的长波辐射却被大气中的二氧化碳等物质所吸收,从而产生大气变暖的效应,二氧化碳过量排放导致大气中二氧化碳含量过高,温度逐渐升高,形成“温室效应”,故A正确;
B.根据分析,过程②中,a极的电极反应为:2C2O524e=4CO2↑+O2↑,该电极反应为氧化反应,故B错误;
C.根据题中信息,可以推出过程③中的反应可表示为:CO2+O2-=CO32-,故C正确;
D.根据分析,熔盐电解池的总的化学方程式为:CO2![]() C+O2,故D正确;
C+O2,故D正确;
答案选B。


 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案科目:高中化学 来源: 题型:
【题目】多相催化反应是在催化剂表面通过吸附、解吸过程进行的。我国学者发现T℃时(各物质均为气态),甲醇与水在铜基催化剂上的反应机理和能量图如图:


下列说法正确的是( )
A.反应Ⅱ的热化学方程式为:CO(g)+H2O(g)=H2(g)+CO2(g) △H=+akJ/mol(a>0)
B.1molCH3OH(g)和1molH2O(g)的总能量大于1molCO2(g)和3molH2(g)的总能量
C.选择优良的催化剂降低反应Ⅰ和Ⅱ的活化能,有利于减少过程中的能耗
D.CO(g)在反应中生成又消耗,CO(g)可认为是催化剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设NA表示阿伏加德罗常数,下列叙述正确的是
A. 13g锌与一定量浓硫酸恰好完全反应,生成气体的分子数为0.2NA
B. 71g氯气通入足量的水中,反应中转移的电子总数为NA
C. 由D和18O所组成的水11g,所含的中子数为4NA
D. 1molBrCl与H2O完全反应生成氯化氢和次溴酸,转移的电子数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是( )。
A.在离子化合物中,只存在离子键,没有共价键
B.非极性键只存在于双原子的单质分子(如![]() )中
)中
C.原子序数为11与9的元素能够形成离子化合物
D.由不同元素组成的含多个原子的分子中,只存在极性键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】2mol金属钠和1mol氯气反应的能量关系如图所示,下列说法不正确的( )

A.△H2+△H3+△H4+△H5+△H6+△H7=△H1
B.△H4的值数值上和Cl-Cl共价键的键能相等
C.△H5<0,在相同条件下,2Br(g)的△H5′<△H5
D.△H7<0,且该过程形成离子键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是(NA表示阿伏加德罗常数的值) ( )
A. 在常温常压下,11.2 L N2含有的原子数为NA
B. 32 g O2在标准状况下所占体积约为22.4 L
C. 标准状况下,18 g H2O所占的体积约为22.4 L
D. 在同温同压下,相同体积的任何气体单质所含的原子数相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图A、B、C、D、E、F等几种常见有机物之间的转化关系图,其中A是面粉的主要成分;C和E反应能生成F,F具有香味。
![]()
在有机物中,凡是具有—CHO结构的物质,具有如下性质:
(1)与新制氢氧化铜悬浊液反应,产生砖红色沉淀;
(2)在催化剂作用下, —CHO被氧气氧化为—COOH,即![]() 。
。
根据以上信息及各物质的转化关系完成下列各题。
(1)B的化学式为_________,C的结构简式为__________。
(2)其中能与新制氢氧化铜悬浊液反应产生砖红色沉淀的物质有_________(填名称)。
(3)C→D的化学方程式为______________。
(4)C + E→ F的化学方程式为 ______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定稳定下,在容积不变的密闭容器中,进行如下可逆反应:![]() ,下列能表明该反应已达到平衡状态的是
,下列能表明该反应已达到平衡状态的是
①![]()
②![]()
③![]()
④混合气的密度保持不变
⑤混合气体的平均摩尔质量不变
A.仅④B.仅④⑤
C.仅①④D.仅③④⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用Cl2生产某些含氯有机物时会生成副产物HCl,利用下列反应可实现氯的循环利用:4HCl(g)+O2(g)![]() 2Cl2(g)+2H2O(g) ΔH=-115.6kJ·mol-1。恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是( )
2Cl2(g)+2H2O(g) ΔH=-115.6kJ·mol-1。恒温恒容的密闭容器中,充入一定量的反应物发生上述反应,能充分说明该反应达到化学平衡状态的是( )
A.气体的质量不再改变
B.氯化氢的转化率不再改变
C.断开4molH—Cl键的同时生成4molH—O键
D.n(HCl)∶n(O2)∶n(Cl2)∶n(H2O)=4∶1∶2∶2
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com