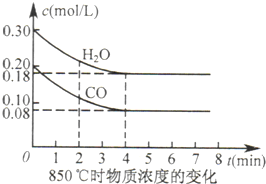
(1)二氧化硫的催化氧化的过程如图1所示,

其中a、c二步的化学方程式可表示为:SO
2+V
2O
5?SO
3+V
2O
44VOSO
4+O
2?2V
2O
5+4SO
3.
该反应的催化剂是______(写化学式)
(2)550℃时,SO
2转化为SO
3的平衡转化率(α)与体系总压强(p)的关系如图2所示.将2.0molSO
2和1.0molO
2置于5L密闭容器中,反应达平衡后,体系总压强为0.10MPa.试计算反应2SO
3?2SO
2+O
2在550℃时的平衡常数K=______.
(3)550℃时,将2.0molSO
2和1.0molO
2置于5L密闭容器中,反应达平衡后,下列措施中能使
增大的是______
A.升高温度B.充入He(g),使体系总压强增大
C.再充入2molSO
2和1molO
2D.再充入1molSO
2和1molO
2(4)维持温度不变条件下使之发生如下反应:2SO
2+O
2?2SO
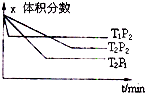
3,有两只密闭容器A和B.A容器有一个可以移动的活塞能使容器内保持恒压,B容器能保持恒容.起始时向这两个容器中分别充入等物质的量的体积比为2:1的SO
2和O
2的混合气体,并使A和B容积相等(如图3所示).
试填写下列空格:
A容器达到平衡时所需的时间比B容器______(填:“短”或“长”);平衡时A容器中SO
2的转化率比B容器______(填:“大”或“小”);达到所述平衡后,若向两容器中通入等物质的量的原反应气体,达到平衡时,A容器的混合气体中SO
3的体积分数______(填“增大”、“减小”或“不变”,下同);B容器的混合气体中SO
3的体积分数______.




 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案