
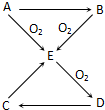
 ��֪A��B��C��D��E������������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�P��Ӧ����δ�г���������ʱ��Ҫ�������������裩��
��֪A��B��C��D��E������������ͼ��ʾ��ת����ϵ�����ַ�Ӧ�P��Ӧ����δ�г���������ʱ��Ҫ�������������裩������ ת����ϵ�У�A��������������Ӧ���ﶼ���Լ�����������Ӧ��˵��A�е�Ԫ���DZ��Ԫ�أ����ڷǽ�����A+O2��E��E+O2��D��D+H2O��C��֤��CΪ�ᣬB+O2��E��E+O2��D��D+H2O��C����A��������Ӧ����B��
��1����AΪ���嵥�ʣ��ƶ�ΪN2����BΪ������EΪһ��������DΪ����������CΪ���
��2����AΪ���嵥�ʣ��������ڶ���̼���ƶ�ΪS����BΪ���⣬EΪ��������DΪ��������CΪ���ᣮ
��� �⣺ת����ϵ�У�A��������������Ӧ���ﶼ���Լ�����������Ӧ��˵��A�е�Ԫ���DZ��Ԫ�أ����ڷǽ�����A+O2��E��E+O2��D��D+H2O��C��֤��CΪ�ᣬB+O2��E��E+O2��D��D+H2O��C����A��������Ӧ����B��
��1����AΪ���嵥�ʣ��ƶ�ΪN2����BΪ������EΪһ��������DΪ����������CΪ���ᣬ
��D��C�ķ�Ӧ�Ƕ���������ˮ��Ӧ���������һ�������ķ�Ӧ����Ӧ�Ļ�ѧ����ʽΪ��3NO2+H2O=2HNO3+NO��
�ʴ�Ϊ��3NO2+H2O=2HNO3+NO��
��C��E�ķ�ӦΪͭ��ϡ���� ��������ͭ��һ��������ˮ����Ӧ�����ӷ���ʽΪ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
�ʴ�Ϊ��3Cu+8H++2NO3-=3Cu2++2NO��+4H2O��
��2����AΪ���嵥�ʣ��������ڶ���̼���ƶ�ΪS����BΪ���⣬EΪ��������DΪ��������CΪ���ᣬ
�ٷ�����֪D�Ļ�ѧʽΪSO3���ʴ�Ϊ��SO3��
��C��E�ķ�ӦΪ�������ƺ�Ũ���ᷴӦ���ɶ������������ͭ��Ũ���ᷴӦ���ɶ����������壬��Ӧ�Ļ�ѧ����ʽΪNa2SO3+H2SO4��Ũ��=Na2SO4+SO2��+H2O��Cu+2H2SO4��Ũ�� $\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
�ʴ�Ϊ��Na2SO3+H2SO4��Ũ��=Na2SO4+SO2��+H2O��Cu+2H2SO4��Ũ�� $\frac{\underline{\;\;��\;\;}}{\;}$CuSO4+SO2��+2H2O��
�۽�Eͨ��ijЩ���ʵ���Һ�У��ɷ�����Ӧ��������ǿ�ᣬ����������Ϊ�������嵥�ʡ��ⵥ�ʵȣ���Ӧ�Ļ�ѧ����ʽΪSO2+Cl2+2H2O=2HCl+H2SO4��
�ʴ�Ϊ��SO2+Cl2+2H2O=2HCl+H2SO4��
���� ���⿼���������ʵ�ת����ϵ���������ʵ�Ӧ�ã���Ҫ�������仯��������仯�������ʵ�Ӧ�ã��Ѷ��еȣ���������Ԫ�ػ�����������ǽ���ؼ���



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ͭ�ۼ����Ȼ�����Һ�У�Cu+Fe3+�TCu2++Fe2+ | |
| B�� | ������Ͷ��ˮ�У�Na+H2O�TNa++OH-+H2�� | |
| C�� | ����������Һ���뵽ϡ�����У�OH-+H+�TH2O | |
| D�� | ʯ��ʯͶ�뵽ϡ�����У�CO32-+2H+�TCO2��+H2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �� | B�� | ������Һ | C�� | ʳ��ˮ | D�� | ������������ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����O2��ȼ������SO2 | B�� | ����O2��ȼ������SO3 | ||
| C�� | ��ķǽ����Ա�����ǿ | D�� | �������ֻ�������� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ����̿�ۺͶ������� | |
| B�� | ������ζ�ķ�������ƺͰ״� | |
| C�� | �ó���ʯ��ˮ�������Ͷ�����̼ | |
| D�� | ����̻��ķ��������ͭƬ��ͭƬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����0.5�������� | B�� | Ħ��������32g/mol | ||
| C�� | ����3.01��1023�������� | D�� | ������16g |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| ʵ�鲽�� | ʵ����� | ʵ������ |
| �� | ����Ӧ��ĺ�ɫ��ĩX���ٶ��ɷֲַ����ȣ�ȡ��������������һ�Թ��У������������ᣬ�� | ��ɫ��ĩ���ܽ⣬��Һ��dz��ɫ�����������ݲ��� |
| �� | ��ʵ����еõ�����Һ�μӼ���KSCN��Һ���� | ��Һû�г��ֺ�ɫ |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com