
在给定的条件下,下列选项所示的物质间转化均能实现的是
A.SiO2  SiCl4
SiCl4  Si
Si
B.FeS2  SO2
SO2 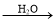 H2SO4
H2SO4
C.N2 NH3
NH3 NH4Cl(aq)
NH4Cl(aq)
D.MgCO3 MgCl2
MgCl2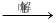 Mg
Mg
 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案 快乐暑假暑假能力自测中西书局系列答案
快乐暑假暑假能力自测中西书局系列答案科目:高中化学 来源:2017届山西省高三上学期10月月考化学试卷(解析版) 题型:选择题
能正确表示下列反应的离子方程式的是
A.用浓盐酸酸化的KMnO4溶液与H2O2反应,证明H2O2具有还原性:2MnO4-+ 6H+ + 5H2O2= 2Mn2+ + 5O2↑ + 8H2O
B.向次氯酸钙溶液通入过量CO2:Ca2++2ClO-+CO2+H2O =CaCO3↓+2HClO
C.向次氯酸钙溶液通入SO2:Ca2++2ClO-+SO2+H2O= CaSO3↓+2HClO
D.FeBr2溶液与等物质的量的Cl2反应:2Fe2++ 2Br-+2Cl2=2Fe3++4Cl-+Br2
查看答案和解析>>
科目:高中化学 来源:2017届河北邯郸市高三上学期第二次月考化学试卷(解析版) 题型:实验题
课题式研究性学习是培养学生创造思维的良好方法.某研究性学习小组将下列装置如图连接,D、F、X、Y 都是铂电极、C、E是铁电极。将电源接通后,向乙中滴入酚酞试液,在F极附近显红色。试回答下列问题:
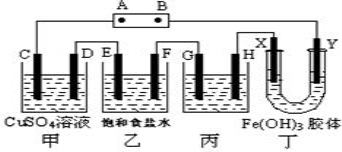
(1)电源B 极的名称是___________。
(2)甲装置中电解反应的总化学方程式是:_________________。
(3)设电解质溶液过量,则同一时间内C、D电极上参加反应的单质或生成的单质的物质的量之比是__________。
(4)欲用丙装置将粗铜(含少量铁、锌等杂质)精炼,G极材料应该是__________(填“粗铜”或“精铜”),电解液中原电解质的物质的量浓度将__________(填“变大”、“变小”或“不变”)。
(5)设甲池中溶液的体积在电解前后都是500ml,当乙池所产生气体的体积为4.48L(标准状况)时,甲池中所生成物质的物质的量浓度为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2017届河北邯郸市高三上学期第二次月考化学试卷(解析版) 题型:选择题
向100mL 0.1mol/L AlCl3 溶液中,加入c mol/L NaOH 溶液100mL后,再滴加1mol/L 盐酸,滴加盐酸的体积与生成沉淀的质量关系如图所示,则加入的NaOH溶液的浓度为( )

A.0.25mol/L B.0.5 mol/L C.2mol/L D.1mol/L
查看答案和解析>>
科目:高中化学 来源:2017届广西省高三上9月月考化学试卷(解析版) 题型:实验题
某小组同学在实验室里对Fe3+与I﹣的反应进行探究,实现Fe3+与Fe2+相互转化.
(1)甲同学首先进行了如下实验:
编号 | 操作 | 现象 |
Ⅰ | 先向2mL0.1mol•L﹣1FeCl2溶液中滴加KSCN溶液,再滴加新制氯水 | ___________________ ___________________ |
Ⅱ | 先向2mL0.1mol•L﹣1FeCl3溶液中滴加KSCN溶液,再滴加0.1mol•L﹣1KI溶液 | 滴加KSCN溶液后,溶液变成血红色;滴加0.1mol•L﹣1KI溶液后,血红色无明显变化 |
实验Ⅰ中发生反应的离子方程式为 , .
(2)实验II的现象与预测不同,为探究可能的原因,甲同学又进行了如下实验,
操作及现象如下:
编号 | 操作 | 现象 |
Ⅲ | 向2mL0.1mol•L﹣1KI溶液中滴加1mL 0.1mol•L﹣1FeCl3溶液,再滴加KSCN溶液 | 滴加FeCl3溶液后,溶液变成黄色;滴加KSCN溶液后,溶液变成血红色 |
根据实验Ⅲ,该同学认为Fe3+有可能与I﹣发生氧化还原反应.请结合实验现象说明得出该结论的理由: .
(3)乙同学认为,还需要进一步设计实验才可证明根据实验Ⅲ中现象得出的结论.
请补全下表中的实验方案:
编号 | 操作 | 预期现象及结论 |
Ⅳ | 向2mL0.1mol•L﹣1KI溶液中滴加1mL 0.1mol•L﹣1 FeCl3,溶液变黄色,取该溶液于两支试管中, 试管①中滴加 , 试管②中滴加 . | 预期现象① , ② . 结论 . |
(4)上述实验结果表明,Fe3+有可能与I﹣发生氧化还原反应.进一步查阅资料知,参加反应的Fe3+和I﹣物质的量相同.该小组同学结合上述实验结论,分析了实验Ⅲ中加入KSCN后溶液变血红色的原因,认为Fe3+与I﹣反应的离子方程式应写为: .
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期第一次月考化学试卷(解析版) 题型:实验题
2015年8月12日天津港特大爆炸事故,再一次引发了人们对环境问题的关注。据查危化仓库中存有大量的钠、钾、白磷(P4)、硝酸铵和氰化钠(NaCN)。爆炸事故中,因爆炸冲击导致氰化钠泄漏,可以通过喷洒双氧水或硫代硫酸钠溶液来处理,以减轻污染。
资料:氰化钠白色结晶颗粒、易潮解、有微弱的苦杏仁气味、剧毒、易溶于水、易水解生成氰化 氢、水溶液呈碱性。
(1)白磷有毒,能和氯酸溶液发生氧化还原反应:3P4 +10HC1O3 +18H2 O=10HC1+12H3 PO4,该反应的氧化产物是 ,若有1 mo1 P4参加反应转移电子为 mol。
(2)氰化钠(NaCN)是一种化工原料,用于基本化学合成、电镀、冶金和有机合成医药、农药及金属处理等方面。
①已知:25℃时,HCN的电离平衡常数Ka = 6.2×10-10,H2CO3在25℃时的电离平衡常数是Ka1=4.5×10-7 Ka2=4.7×10-11,则向NaCN溶液通入少量CO2反应方程式是: 。
②常温下,氰化钠能与过氧化氢溶液反应,生成碳酸氢钠和能使湿润的红色石蕊试纸变蓝色的气体,大大降低其毒性。该反应的化学方程式是: 。
(3)实验室通过如图所示装置制备Na2SO3。

装置a中盛装Na2SO3固体的仪器名称是 ;装置b的作用是 。
(3)装置c中的产物有Na2S2O3和CO2气体等,实验结束后,装置d中的溶质有NaOH、Na2CO3,还可能有 。
(4)实验结束后,在e处最好连接盛 (选填“NaOH溶液”、“水”、“CC14”中任一种。
查看答案和解析>>
科目:高中化学 来源:2017届甘肃省高三上学期第一次月考化学试卷(解析版) 题型:选择题
三氟化氮(NF3)是微电子工业中一种优良的等离子蚀刻气体,它无色、无臭,在潮湿的空气中能发生下列反应:3NF3+5H2O=2NO+HNO3+9HF,下列有关说法正确的是( )
A.反应中NF3是氧化剂,H2O是还原剂
B.NF3在潮湿空气中泄漏会产生白雾、红棕色气体等现象
C.若反应中生成0.2 mol HNO3,则反应共转移0.2 mol e-
D.反应中被氧化与被还原的原子物质的量之比为2:1
查看答案和解析>>
科目:高中化学 来源:2017届浙江省高三上学期10月月考化学试卷(解析版) 题型:计算题
将一定质量Na2CO3和NaHCO3的均匀混合物分成两等份。其中一份直接加热至恒重,质量减轻了1.24g;另一份加入40mL某浓度盐酸恰好完全反应,生成标准状况下气体2.24L。
试计算:
⑴混合物中的NaHCO3物质的量为 mol。
⑵盐酸的浓度为 mol/L。
查看答案和解析>>
科目:高中化学 来源:2017届云南省高三上学期第二次月考化学试卷(解析版) 题型:推断题
[选修5——有机化学基础]
龙胆酸甲酯是制取抗心律失常药物——氟卡尼的中间体。
I.已知龙胆酸甲酯结构如图所示。
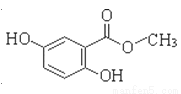
(1)龙胆酸甲酯的分子式为 ,它的含氧官能团名称为
(2)下列有关龙胆酸甲酯的描述,不正确的是______(填字母)
A.不能发生消去反应 B.难溶于水
C.能与溴水反应 D.能与碳酸钠溶液反应产生二氧化碳
(3)龙胆酸甲酯与足量氢氧化钠溶液反应的化学方程式是____________________
II.已知X及其他几种有机物存在如下转化关系,且测得A中含三个甲基:

回答以下问题:
(4)X的结构简式为______________________
(5)写出满足下列条件的龙胆酸的一种同分异构体的结构简式 __________________
①能发生银镜反应 ②能使FeCl3溶液显色 ③酯类 ④苯环上的一氯代物只有两种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com