
【题目】氯化亚铁是重要的还原剂,常用于检测硒、生产聚合氯化铝铁絮凝剂。制备FeCl2的方法有多种。请回答下列问题:
Ⅰ.结晶法制取FeCl2
在一定浓度的盐酸中,逐渐加入过量的铁屑,充分反应后,蒸发至出现晶膜,____,______,固液分离,洗涤,快速干燥制得。
Ⅱ.氯苯还原无水FeC13制取FeC12
无水FeCl3与氯苯反应的化学方程式为:2FeCl3+C6H5Cl![]() 2FeCl2+C6H4Cl2+HCl↑
2FeCl2+C6H4Cl2+HCl↑
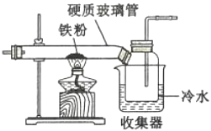
(1)如图是用干燥的C12和铁粉制取无水FeC13的装置。硬质玻璃管和收集器用大口管连接的原因是________。
(2)利用如图装置制备无水FeC12,并检测FeC13的转化率。已知相关物质的部分性质如下:

C6H5C1(氯苯) | C6H4C12 | FeC13 | FeC12 | |
相对分子质量 | 112.5 | 147 | 162.5 | 127 |
熔点/℃ | -45 | 53 | 306 | 670~674 |
沸点/℃ | 132 | 173 | 315 | 1023 |
将162.5 g无水氯化铁和200 g氯苯加入到圆底烧瓶中,在锥形瓶中加入200 g滴有酚酞的9.5%的NaOH溶液。先通入N2一段时间,再加热,控制温度在132 ℃左右发生反应。实验完成后冷却,分离提纯得到粗产品。
①先通入N2的目的是_______;导管a的作用是______。
②当锥形瓶内溶液颜色由红色变为无色时,停止加热,则氯化铁转化率理论上达到或超过______%。
③实验结束后,回收过量氯苯的操作名称为______。
④指出装置c可能存在的缺点______。
【答案】趁热过滤 (冷却)结晶 FeC13的熔沸点低,防止FeC13冷凝时堵塞导管 除尽装置中的O2和水蒸气,防止FeCl2被氧化、防止发生水解反应 导气,冷凝回流氯苯 95 蒸馏 无防倒吸装置
【解析】
I.在一定浓度的盐酸中,逐渐加入过量的铁屑,充分反应后,蒸发至出现晶膜,趁热过滤、冷却结晶、固液分离,洗涤,快速干燥制得FeCl2;
II.(1)FeCl3熔沸点低,冷凝时易堵塞导管;
(2)在装置b中发生反应:2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl,由于Fe2+具有强的还原性,易被空气氧化,先通入N2,排出装置内空气,就可以避免副反应产生的干扰,导气管a同时起导气和冷凝作用,反应产生的HCl被锥形瓶中的NaOH溶液吸收,根据二者反应关系计算产生的HCl的物质的量,进而可知反应的FeCl3的量,结合加入反应物的量计算其转化率。
I.在一定浓度的盐酸中,逐渐加入过量的铁屑,充分反应后,蒸发至出现晶膜,趁热过滤、冷却结晶、固液分离,洗涤,快速干燥制得FeCl2;
II.(1)用干燥的Cl2和铁粉制取无水FeCl3,硬质玻璃管和收集器用大口管连接的原因是FeCl3熔沸点低,防止FeCl3冷凝时堵塞导管;
(2)①先通入N2的目的是排出装置中空气,防止空气中的O2氧化FeCl2变为FeCl3,同时也可以避免反应产生的Fe3+发生水解反应;装置中导管a的作用是导气和冷凝,可以使挥发的未反应的氯苯回流到反应装置;
②n(FeCl3)=![]() =1 mol,n(C6H5C1) =
=1 mol,n(C6H5C1) =![]() =1.78 mol,根据方程式2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl可知二者反应时的物质的量的比是2:1,n(FeCl3):n(C6H5C1)<2:1,说明氯苯过量,反应根据FeCl3的物质的量计算,n(HCl)=n(NaOH)=
=1.78 mol,根据方程式2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl可知二者反应时的物质的量的比是2:1,n(FeCl3):n(C6H5C1)<2:1,说明氯苯过量,反应根据FeCl3的物质的量计算,n(HCl)=n(NaOH)=![]() =0.475 mol,根据反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl可知氯化铁转化率为:
=0.475 mol,根据反应2FeCl3+C6H5Cl→2FeCl2+C6H4Cl2+HCl可知氯化铁转化率为:![]() ×100%=95%;
×100%=95%;
③实验结束后,在装置b中含有过量的氯苯及反应产生的二氯苯,由于氯苯、二氯苯是互溶的沸点不同的液体混合物,所以分离二者混合物,回收其中过量氯苯的操作方法为蒸馏;
④由于HCl气体极易溶于水,并且会与c中NaOH反应,使装置中气体压强过小而引起倒吸现象,因此装置c可能存在的缺点是无防倒吸装置。


科目:高中化学 来源: 题型:
【题目】某化学小组为了证明二氧化硫和氯气的漂白性,设计了如下图所示的实验装置:

他们制备二氧化硫和氯气所依据的原理分别是:
Na2SO3+H2SO4 = Na2SO4+H2O+SO2↑
MnO2+4HCl(浓) ![]() MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
(1)用来制取氯气的装置是______(填字母),反应中浓盐酸所表现出________________性质。
(2)反应开始一段时间后,B、D试管中的品红溶液均退色。停止通气后,再给B、D两个试管分别加热____ (填" B”或“D")试管中无明显现象。
(3)装置C的作用是________________________;
(4)若装置D中的品红溶液换成紫色的石蕊溶液,则出现的现象是____________________________;
(5)该小组同学将两种气体混合后通入品红溶液,一段时间后,品红溶液几乎不退色。查阅资料得知:两种气体按体积比1:1混合,再与水反应可生成两种常见的酸,因而失去漂白作用,该反应的化学方程式是:________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】维纶(聚乙烯醇缩甲醛纤维)可用于生产服装、绳索等。其合成路线如下:

下列说法不正确的是
A.反应①是加聚反应
B.高分子A的链节中只含有一种官能团
C.通过质谱法测定高分子B的平均相对分子质量,可得其聚合度
D.反应③的化学方程式为:![]() +nHCHO→
+nHCHO→![]() +(2n-1)H2O
+(2n-1)H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向1 mol·L-1NH4C1溶液中加入足量的镁条,该体系pH随时间变化的曲线如图所示。实验观察到b点开始溶液中有白色沉淀生成。下列说法错误的是( )(已知Ksp[Mg(OH)2]=1.8×10-11)

A.a点溶液中,c(NH4+)+c(H+)<c(C1-)+c(OH-)
B.b点时,溶液中c(Mg2+)=0.18 mol·L-1
C.体系中,水的电离程度大小关系为a>c>b
D.常温下,NH4C1的水解平衡常数数量级为10-10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】以不同类别物质间的转化为线索,认识钠及其化合物。

下列分析不正确的是
A.反应③表明CO2具有酸性氧化物的性质
B.反应④说明NaHCO3的稳定性强于Na2CO3
C.反应⑤、⑥可用于潜水艇中氧气的供给
D.上述转化中发生的反应有分解反应、化合反应、置换反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】实验室中有一未知浓度的稀盐酸,某学生为测定盐酸的浓度在实验室中进行如下实验:请完成下列填空:
(1)配制100mL 0.1000mol/L NaOH标准溶液。
(2)取20.00mL待测稀盐酸溶液放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用自己配制的标准NaOH溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
实验编号 | NaOH溶液的浓度(mol/L) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测盐酸溶液的体积(mL) |
1 | 0.1000 | 30.05 | 20.00 |
2 | 0.1000 | 29.95 | 20.00 |
3 | 0.1000 | 28.20 | 20.00 |
①滴定达到终点的判断是__。
②根据上述数据,可计算出该盐酸的浓度约为___________(保留两位小数)。
③排去碱式滴定管中气泡的方法应采用操作______,然后轻轻挤压玻璃球使尖嘴部分充满碱液。
甲.![]() 乙.
乙.![]() 丙.
丙.![]()
④在上述实验中,下列操作(其他操作正确)会造成盐酸浓度测定结果偏高的有_____。
A.碱式滴定管使用前,水洗后未用NaOH标准溶液润洗
B.锥形瓶水洗后未干燥
C.滴定前读数时正确,滴定后俯视刻度线
D.碱式滴定管尖嘴部分有气泡,滴定后消失
⑤如图是某次滴定时的滴定管中的液面,其读数为__________mL。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现在含有生命元素硒(![]() )的保健品已经进入市场,已知硒与氧同族,与钾同周期,则下列关于硒的叙述中正确的是( )
)的保健品已经进入市场,已知硒与氧同族,与钾同周期,则下列关于硒的叙述中正确的是( )
A.硒单质在常温下是固体
B.硒的气态氢化物稳定性比![]() 强
强
C.硒是金属元素
D.硒酸(![]() )的酸性比硫酸强
)的酸性比硫酸强
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“索尔维制碱法”工艺流程如图所示,请回答下列问题:
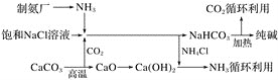
(1)向饱和氯化钠溶液中先通入___,效果更好。反应制得NaHCO3沉淀和NH4Cl溶液的化学方程式为____。
(2)索尔维制碱法除了得到纯碱外,还会产生一种废渣___。侯氏制碱法在此工艺上改进,不再使用碳酸钙制备CO2,而是在制备NH3的过程中制得CO2,则侯氏制碱法在得到纯碱的同时还制得了___,此物质在农业上的用途是___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】烯烃是重要的有机化合物.其中乙烯是最简单的一种烯烃,其产量代表着一个国家石油化工产业的水平。
完成下列问题:
(1)实验室用如图所示装置制取乙烯,反应方程式是____,无水乙醇与浓硫酸的体积比为1:3,请解释加入浓硫酸不宜过少的原因是__。
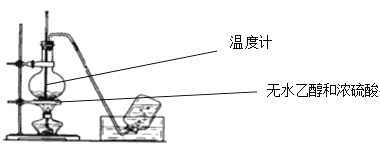
(2)反应需要迅速升温至所需温度的理由是___。所以烧瓶中应放入的固体物质是___,其作用是____。
(3)烯烃通过催化加氢可以得到烷烃。请写出一种可以通过催化加氢反应得到2,2-二甲基丁烷的结构简式:___。
(4)有一种烷烃A,分子式C9H20,它却不能由任何C9H18的烯烃催化加氢得到。请写出A的结构简式___,在A的同分异构体中,却存在只能由1种烯烃催化加氢得到的烷烃,请写出一种符合要求的A的同分异构体的结构简式:___。
烯烃还可以与卤素单质、卤化氢、水发生加成反应,产物有主次之分,例如:
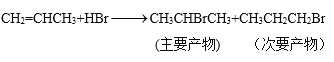
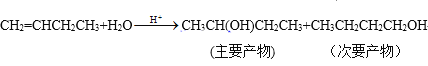
(5)化学式为C4H8的某烃A与HBr加成得到的主要产物,其一氯代物只有一种,请写出A发生聚合反应的方程式:___。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com