
| 质量 | 实验前 | 实验后 |
| 药品+U形管的质量/g | 101.1 | 102.9 |
| 药品+广口瓶D的质量/g | 312.0 | 314.2 |
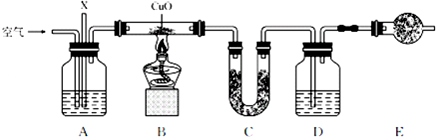
分析 (1)由于空气中含有CO2,会干扰燃烧产物CO2的吸收,所以必须利用氢氧化钠除去空气中的CO2.其次还可以利用A中气泡的产生的快慢来可知通入通入速率,以保证O2过量;
(2)D是吸收CO2的,所以盛放的试剂是浓NaOH溶液;
(3)由于空气中也含有水蒸气和CO2,所以E装置是吸收空气中的水和CO2的,因此试剂是碱石灰或固体NaOH;
(4)由于从A中出来的气体中一定含有水蒸气,会对后续的实验产生影响,所以需要在A和B之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管;
(5)药品+U形管的质量/g增加1.8 g为生成水的质量,广口瓶D质量增加2.2g为燃烧生成二氧化碳气体的质量,物质的量分别是0.1mol水和0.05mol二氧化碳,计算得到碳和氢元素的质量之比.
解答 解:(1)由于空气中含有CO2,会干扰燃烧产物CO2的吸收,所以必须利用氢氧化钠除去空气中的CO2.其次还可以利用A中气泡的产生的快慢来可知通入通入速率,以保证O2过量;
故答案为:除去空气中的CO2气体; 调节X和空气的通入速率,保证O2过量;
(2)D是吸收CO2的,所以盛放的试剂是浓NaOH溶液,故答案为:浓NaOH溶液;
(3)由于空气中也含有水蒸气和CO2,所以E装置是吸收空气中的水和CO2的,因此试剂是碱石灰或固体NaOH;
故答案为:防止空气中的二氧化碳和水蒸气进入装置D,对结果产生影响;
(4)由于从A中出来的气体中一定含有水蒸气,会对后续的实验产生影响,所以需要在A和B之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管,
故答案为:在A、B 之间加一个盛浓硫酸的洗气瓶或盛无水CaCl2(或P2O5、碱石灰、固体NaOH等)的干燥管;
(5)药品+U形管的质量/g增加1.8 g为生成水的质量,广口瓶D质量增加2.2g为燃烧生成二氧化碳气体的质量,物质的量分别是0.1mol水和0.05mol二氧化碳,其中碳和氢元素的质量之比=0.05×12:0.1×2×1=3:1,
故答案为:3:1.
点评 本题考查有机物分子式及结构简式的判断,实验过程中装置和试剂的选择和作用分析判断,有机物的组成计算分析应用,掌握实验基础和燃烧实验的定量计算测定方法是解题关键,题目难度中等.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:选择题
| A. | Cu2+、Cl-、SO42-、K+ | B. | K+、OH-、CO32-、Na+ | ||
| C. | HCO3-、OH-、Cl-、Na+ | D. | Ag+、NO3-、Cl-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 某溶液中滴入AgNO3溶液,生成白色沉淀,该溶液中可能含Cl- | |
| B. | 实验已经证明,氯水是可以导电的,所以氯水是电解质 | |
| C. | 某溶液与淀粉碘化钾溶液反应后出现蓝色,则证明该溶液是氯水 | |
| D. | 胶体与其它分散系的本质区别在于胶体具有丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
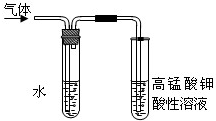 实验室制备溴乙烷并进行溴乙烷的性质实验如下,试回答下列问题:
实验室制备溴乙烷并进行溴乙烷的性质实验如下,试回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 若8>m>3,则X必定为主族元素 | |
| B. | 若Y的气态氢化物化学式为YHn,且b<4,则该氢化物为极性分子 | |
| C. | 若a<b<m=n=4,则晶体类型相同时,其单质熔点:Y>X | |
| D. | 若a=b=3,8>m>n>b,则元素非金属性:X>Y |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com