
【题目】为了除去括号内的杂质,其试剂选择和分离方法都正确的是( )
序号 | 物质(杂质) | 所用试剂 | 分离方法 |
A | 甲烷(乙烯) | 溴水 | 洗气 |
B | 氢氧化钠溶液(氢氧化钙溶液) | 二氧化碳 | 过滤 |
C | 乙烯(SO2) | 酸性KMnO4 | 洗气 |
D | CO2(HCl) | 饱和Na2CO3溶液 | 洗气 |
A. A B. B C. C D. D
 优学名师名题系列答案
优学名师名题系列答案科目:高中化学 来源: 题型:
【题目】从化学键的观点看,化学反应的实质是“旧键的断裂,新键的形成”,据此你认为下列变化属于化学反应的是( )
A. 对空气进行降温加压 B. 金刚石变成石墨
C. NaCl熔化 D. 碘溶于CCl4中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
化合物H是一种有机光电材料中间体。实验室由芳香化合物A制备H的一种合成路线如下: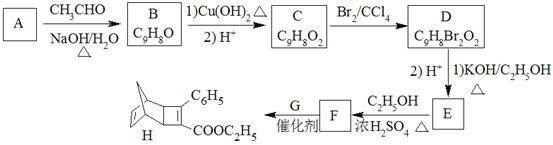
已知:
![]()
![]()
回答下列问题:
(1)A的化学名称为为__________。
(2)由C生成D和E生成F的反应类型分别为__________、_________。
(3)E的结构简式为____________。
(4)G为甲苯的同分异构体,由F生成H的化学方程式为___________。
(5)芳香化合物X是F的同分异构体,X能与饱和碳酸氢钠溶液反应放出CO2,其核磁共振氢谱显示有4种不同化学环境的氢,峰面积比为6∶2∶2∶1,写出2种符合要求的X的结构简式____________。
(6)写出用环戊烷和2-丁炔为原料制备化合物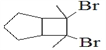 的合成路线________(其他试剂任选)。
的合成路线________(其他试剂任选)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】由氮的化合物引起的环境污染称为氮污染。
(1)己知CO将NO转化为N2的方程式为2CO(g)+2NO(g)![]() N2(g)+2CO2(g) ΔH,某研究小组在实验中研究温度对NO转化率的影响并绘制图像。
N2(g)+2CO2(g) ΔH,某研究小组在实验中研究温度对NO转化率的影响并绘制图像。
①当n(NO)/n(CO)=l,容器容积恒定时,在不同温度下反应相同的时间测得NO的转化率变化如图所示,则在此反应时间内应控制反应的最佳温度在______左右,该反应的ΔH_____0 (填>或<)。

②该反应的平衡常数表达式为K=__________。
要同时提高平衡常数的值和NO的平衡转化率,可采取的措施是________。
A.降低温度 B.及时将CO2和N2从反应体系中移走
C.升高温度 D.增大压强
③在恒温恒容容器中按体积比2∶1充入CO和NO的混合气体,下列选项能说明正反应速率大于逆反应速率的是_____________(填序号)。
A.CO的浓度保持恒定 B.混合气体的平均相对分子质量逐渐减小
C.CO和NO的物质的量之比逐渐增大 D.CO、NO、N2的速率之比为2∶2∶1
(2)在催化剂存在的条件下,用H2可以将NO还原为N2,己知:

则氢气和一氧化氮反应生成氮气和水蒸气的热化学方程式是_________________。
(3)MAP沉淀法是一种比较新颖有效的处理氨氮废水的方法,.原理如下:向含NH4+的废水中投加磷酸盐和镁盐,使之和NH4+生成难溶复盐MgNH4PO4·6H2O (简称MAP)。MAP沉淀法需要控制反应的PH在7.5-10之间,当PH过高时不利于生成MAP的原因是____________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】已知:2H2(g)+O2(g)=2H2O(g),1molH2完全燃烧放出热量241.8KJ,有关键能数据如下:
化学键 | H-O | O=O |
键能/kJmol﹣1 | 463.4 | 498 |
则H﹣H键键能为( )
A. 413 kJ/mol B. 557 kJ/mol C. 221.6 kJ/mol D. 436 kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列物质分类正确的是
A. Cu(OH)2难溶于水,属于非电解质
B. SO2能与碱反应生成盐和水,属于酸性氧化物
C. NH4Cl组成中不含金属离子,不属于盐
D. HCl气体溶于水电离成H+和Cl-,属于离子化合物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将一块铁片放入0.5L 1mol/L CuSO4溶液中,反应一段时间后,取出铁片,小心洗净后干燥称量,铁片增重0.8g,则反应后溶液中CuSO4的物质的量浓度是(反应前后溶液的体积不变)
A. 0.9 mol/L B. 0.85 mol/L C. 0.8 mol/L D. 0.75 mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com