
下列说法正确的是()
A. 1mol任何气体所含分子数都相同,体积也都约为22.4 L
B. 1molKClO3和1molSO2中,所含氧原子的个数比为3:2
C. 物质的量就是物质的摩尔质量
D. 在非标准状况下,1 mol任何物质的体积都不是22.4 L
考点: 气体摩尔体积;摩尔质量.
专题: 阿伏加德罗常数和阿伏加德罗定律.
分析: A、标准状况下,1mol任何气体体积都约为22.4 L;
B、根据化学式求出O原子的物质的量,再求比值;
C、根据物质的量及摩尔质量的概念分析;
D、一定条件下,1 mol气体的体积可能是22.4 L.
解答: 解:A、标准状况下,1mol任何气体所含分子数都相同为NA个,体积也都约为22.4 L,不是标准状况是无法确定,故A错误;
B、1molKClO3含氧原子为3mol,1molSO2中含氧原子为2mol,则1molKClO3和1molSO2中,所含氧原子的个数比为3:2,故B正确;
C、物质的量表示含有一定数目粒子的集合体,单位物质的量的物质所具有的质量称为摩尔质量,则二者不是同一概念,故C错误;
D、一定条件下,只要温度与压强合适,1 mol气体的体积可能是22.4 L,故D错误;
故选B.
点评: 本题考查了物质的量、摩尔质量等概念的理解和应用,题目难度不大,侧重于基础知识的考查.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
在长途运输香蕉、苹果、橙子等新鲜水果时,常常在盛放水果的集装箱里放置浸泡有KMnO4酸性溶液的硅藻土,其中KMnO4酸性溶液的作用是( )
|
| A. | 杀死细菌,防止水果腐烂 |
|
| B. | 吸收氧气,防止水果被氧化变色 |
|
| C. | 吸收水果产生的乙烯,防止水果早熟 |
|
| D. | 除去有害气体,防止水果被污染 |
查看答案和解析>>
科目:高中化学 来源: 题型:
铝生产产业链由铝土矿开采、氧化铝制取、铝的冶炼和铝材加工等环节构成。请回答下列问题:
(1)工业上采用电解氧化铝—冰晶石(Na3AlF6)熔融体的方法冶炼得到金属铝:2Al2O3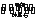 4Al+3O2↑
4Al+3O2↑
加人冰晶石的作用是_____________________。
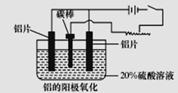
(2)上述工艺所得铝材中往往含有少最Fe和Si等杂质,可用电解方法进一步提纯,该电解池中阳极的电极反应式为_____________,下列可作阴极材料的是____________(填字母序号)。
A.铝材 B.石墨 C.铅板 D.纯铝
(3)阳极氧化能使金属表面生成致密的氧化膜。以稀硫酸为电解液,铝阳极发生的电极反应式为__________。
(4)在铝阳极氧化过程中,需要不断地调整电压,理由是______________________________。
(5)下列说法正确的是(填字母序号)。
A.阳极氧化是应用原电池原理进行金属材料表面处理的技术
B.铝的阳极氧化可增强铝表面的绝缘性能
C.铝的阳极氧化可提高金属铝及其合金的耐腐蚀性,但耐磨性下降
D.铝的阳极氧化膜富有多孔性,有很强的吸附性能,能吸附染料而呈各种颜色
查看答案和解析>>
科目:高中化学 来源: 题型:
X、Y、Z、M、W为原子序数依次增大的5种短周期元素。X的质子总数与电子层数相同,Y、Z、M同周期且相邻,W原子核外电子数是M原子最外层电子数的2倍。Z与其同主族的短周期元素可形成常见气体甲。X、Y、Z 3种元素形成化合物乙。下列说法不正确的是 ( )
A.原子半径:W>Y>Z>M>X B.化合物乙中一定只有共价键
C.由W元素形成的单质以及W与Z两元素形成的化合物都是原子晶体
D.X分别与Y、Z、M、W形成的常见化合物中,稳定性最好的是XM,沸点X2Z>XM
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质在水溶液中电离,其电离方程式错误的是()
A. Al2(SO4)3=2Al3++3(SO4)2﹣ B. NaHSO4=Na++H++SO42﹣
C. MgCl2=Mg2++Cl2﹣ D. Ba(OH)2=Ba2++2OH﹣
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应属于非氧化还原反应的是()
A. Fe2O3+3CO 2Fe+3CO2 B. NH4NO3
2Fe+3CO2 B. NH4NO3 N2O↑+2H2O
N2O↑+2H2O
C. CaCO3 CaO+CO2 D. 4CuO
CaO+CO2 D. 4CuO 2Cu2O+O2↑
2Cu2O+O2↑
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com