
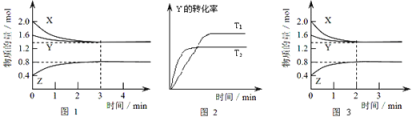
����Ŀ��T��ʱ��2L�ܱ�������ʹX(g)��Y(g)������Ӧ����Z(g)����Ӧ������X��Y��Z��Ũ�ȱ仯��ͼ1��ʾ�������������������䣬�¶ȷֱ�ΪT1��T2ʱ��Y��ת������ʱ��Ĺ�ϵ��ͼ2��ʾ�������н��۲���ȷ���ǣ� ��
A.�����з����ķ�Ӧ�ɱ�ʾΪ��3X(g)+Y(g)![]() 2Z(g)
2Z(g)
B.��Ӧ���е�ǰ3min�ڣ���X��ʾ�ķ�Ӧ����v(X)=0.3mol/(L��min)
C.���������������䣬�����¶ȣ���Ӧ�Ļ�ѧƽ�ⳣ��K��С
D.���ı䷴Ӧ������ʹ��Ӧ������ͼ3��ʾ����ı��������ʹ�ô���
���𰸡�B
��������
A����ͼ1֪��X�����ʵ���������Ϊ(2.0-1.4)mol=0.6mol��Y�����ʵ���������Ϊ(1.6-1.4)mol=0.2mol��X��YΪ��Ӧ�Z�����ʵ���������Ϊ(0.8-0.4)mol=0.4mol��ZΪ�����ͬһ��ѧ��Ӧͬһʱ����ڣ���Ӧ����ٵ����ʵ��������������ӵ����ʵ���֮�ȵ����������֮�ȣ�����X��Y��Z�ļ�����֮��=0.6mol��0.2mol��0.4mol=3��1��2�����Է�Ӧ�ɱ�ʾΪ��3X(g)+Y(g)2Z(g)����A��ȷ��
B����Ӧ���е�ǰ3min�ڣ���X��ʾ�ķ�Ӧ����v(X)= =0.1mol/(L��min)����B����
=0.1mol/(L��min)����B����
C����ͼ2֪�����ȹ���ƽ��ֵ����������T2��T1�������¶ȣ�Y��ת���ʼ��٣�ƽ�����淴Ӧ�����ƶ������������¶ȣ�ƽ�ⳣ����С����C��ȷ��
D��ͼ3��ͼ1�Ƚϣ�ͼ3����ƽ�����õ�ʱ��϶̣�˵����Ӧ��������ƽ��״̬û�з����ı䣬˵�����Ǹı��¶ȵĽ�����÷�Ӧ����Ӧ���������ʵ�����С�ķ�Ӧ��Ҳ���Ǹı�ѹǿ(��Ũ��)�Ľ����Ӧ�Ǽ�������Ľ������D��ȷ��
��ѡB��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼΪһ��������ͼ����С����ͼ���Ϸֱ�д��H2��CO2��Na2O��NaCl��FeCl3�������ʣ�ͼ���������������ʾ��ɹ���Ϊһ�࣬�ཻ����A��B��C��DΪ����Ӧ�ķ������ݴ��š���ش��������⣺
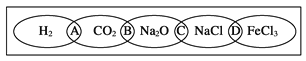
��1���뽫�������ݴ���������Ӧ�������ڣ�
��_______________���������ʶ����ǵ����
��________________���������ʶ�����
��2���ýྻ���ձ�ȡ��������ˮ���þƾ��Ƽ��������ڣ����ձ�����μ��뱥�͵�ͼ��ij������M����Һ�������ʺ��ɫ��
������M�Ļ�ѧʽΪ________________��
��֤���к��ɫ�������ɵ�ʵ�������____��
����Ӧ��
A��2F2��2H2O��4HF��O2���� B��2Na��2H2O��2NaOH��H2����
C��CaO��H2O��Ca(OH)2�� D��2H2O��2H2����O2����
����ˮֻ������������______������ţ�����ӦB�б�������Ԫ��������________��
����Ӧ��3Cu + 8HNO3 = 3Cu(NO3)2+2NO��+4H2O, �����ڸ÷�Ӧ�е�������______ ��ԭ���������������ʵ���֮�ȣ�__________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪����R-NO2![]() R-NH2���ڱ�����ԭ�е�ȡ�������µ����ȡ�������뱽����λ��������Ӱ�졣�������ñ���ԭ���Ʊ�һϵ�л������ת����ϵͼ��
R-NH2���ڱ�����ԭ�е�ȡ�������µ����ȡ�������뱽����λ��������Ӱ�졣�������ñ���ԭ���Ʊ�һϵ�л������ת����ϵͼ��

(1)Aת��ΪB�Ļ�ѧ����ʽ��______________________________��
(2)ͼ����������������ʡ���˷�Ӧ��������д���٢����ʵĽṹ��ʽ����__________����_______��
(3)���Ķ��ȴ�����________��ͬ���칹�塣
(4)�л��� ������ԭ��________(������������������)��ͬһƽ���ϡ�
������ԭ��________(������������������)��ͬһƽ���ϡ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����A��B��C��D��E����Ԫ�أ�����A��B��C����ͬһ���ڣ�Aԭ�������p�ܼ��ĵ��������ڴ����ĵ���������BԪ�ؿɷֱ���A��C��D��E����RB2�ͻ������֪��DB2��EB2�У�D��B��������Ϊ7��8��E��B��������Ϊ1��1�����������������ش��������⣺
��1���ƶ�C��D��EԪ�طֱ���(��Ԫ�ط��Żش�)��C____��D___��E___��
��2��д��Dԭ�ӵĵ����Ų�ʽ____��
��3��д��AԪ����B����ȫȼ�յĻ�ѧ����ʽ_____��
��4��ָ��EԪ����Ԫ�����ڱ��е�λ��____��
��5���Ƚ�A��B��C����Ԫ�صĵ�һ�����ܵĴ�С˳��___(���ɴ�С��˳������,��Ԫ�ط��ű�ʾ)��
��6���Ƚ�Ԫ��D��E�ĵ縺�Ե���Դ�С___��(���ɴ�С��˳�����У���Ԫ�ط��ű�ʾ)��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����ӹ�ҵ���ù�����FeCl3��Һ�ܽ��·���е�ͭ��ʱ�������������Һ���ɸ÷�Һ����ͭ���õ���ˮ����FeCl36H2O���IJ������£�
I.�ڷ�Һ�м���������ۣ����ˣ�
II.��I�������м�������Լ�A����ַ�Ӧ���ˣ��õ�ͭ��
III.�ϲ�I��II�е���Һ��ͨ������������
IV.�������õ�FeCl36H2O���塣
��1����FeCl3��Һ��ʴͭ�������ӷ���ʽ��_____________��
��2���Լ�A��______��
��3��ȡ��������III���õ���Һ���Թ��У��ܹ�֤��ͨ��������������______��
a. ����Cl2�Ĵ��� b. ����Fe3+�Ĵ��� c. ����Fe2+�IJ�����
��4����ɲ���IV��Ҫ�õ���ʵ��װ����______������ĸ����
a b
b c
c d
d
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���мס���������ȫ��ͬ��װ�ã��ֱ������ǵIJ����װ��1.06g Na2CO3��0.84g NaHCO3���Թ��и���10mL��ͬŨ�ȵ����ᣨ��ͼ����ͬʱ����������е�����ȫ��������Ե��Թ��У�����������ȷ����
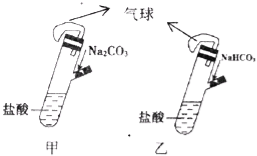
A. ��װ�õ������������ʴ�
B. �����������������ͬ����һ����c��HCl����2 mol/L
C. �����������������ͬ����һ����c��HCl����1 mol/L
D. ��������Һ��Na+��Cl�������ʵ�����ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij����С��ͬѧ�����ͼʵ��װ�ã����ּг�����δ������̽�������Ļ�ԭ�Բ����鲿�ֲ��
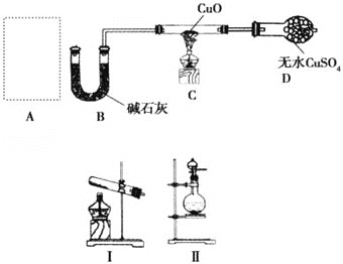
��1����A��ʹ��װ�â���ȡ��������ѧ����ʽΪ__������װ���Թܿ���������б��ԭ��_____����A��ʹ��װ�â���ȡ���������Һ©���е��Լ�Ϊ__��Բ����ƿ�еĹ������Ϊ__��
��2��B�м�ʯ�ҵ�������__��
��3��������ԭ��������ͭ�Ļ�ѧ����ʽΪ__��װ��C�е�ʵ������Ϊ__��װ��D�е�ʵ������Ϊ__��
��4���ٸ�װ�ô������Ե�ȱ����__��
���뻭���Ľ�����Ҫ�������ӵ�ʵ��װ��ͼ________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��(1)��7.8gþ���Ͻ�ķ�ĩ��������������У��õ�8.96 LH2����״���£����úϽ���������NaOH��Һ������H2���������״���£�Ϊ____________ ��
(2)��ͬ�����£�ijCl2��O2�������75mLǡ����100mL H2��������HCl��H2O�����������ƽ����Է�������Ϊ____________��
(3)������ͬ�ݻ����ܱ�����X��Y����25 ���£�X�г���a g A���壬Y�г���a g CH4���壬X��Y�ڵ�ѹǿ֮����2��5����A��Ħ������Ϊ____________��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com