
| A. | 溴乙烷 | B. | 乙烯 | C. | 乙醇 | D. | 甲苯 |
分析 卤代烃、醛、羧酸、醇类、苯的同系物都是分子晶体,熔沸点与相对分子质量成正比,含有氢键的物质熔沸点升高,常温下,苯的同系物都是液态,羧酸、醇类物质都是液态,除了甲醛为其它醛类物质呈液态,一氯甲烷为气态,其它为液态.
解答 解:A、常温常压下,除了一氯甲烷为气体,随着碳原子数的增多和卤素原子的相对分子质量的增大,熔沸点升高,故溴乙烷为液态,故A错误;
B、乙烯在常温常压下为气体,故B正确;
C、由于醇分子间存在氢键,故熔沸点比相同碳原子数的烃高,故乙醇为液态,故C错误;
D、碳原子数大于等于5的烃类均为液态,故甲苯在常温常压下为液态,故D错误.
故选B.
点评 本题以物质状态为载体考查晶体熔沸点比较,明确分子晶体熔沸点高低影响因素是解本题关键,注意化学键不影响熔沸点而影响物质稳定性,为易错点,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | C2H6O | B. | CH3O | C. | C4H12O2 | D. | C5H10O4 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
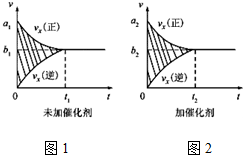
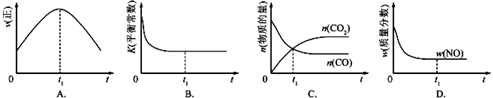
| 温度/℃ | 800 | 1000 | 1200 | 1400 |
| 平衡常数 | 0.45 | 1.92 | 276.5 | 1771.5 |
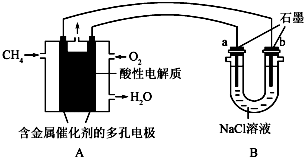
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 一 | H | |||||||
| 二 | C | N | F | Ne | ||||
| 三 | Na | Al | P | S |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4 | B. | 5 | C. | 6 | D. | 7 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 电子数相同的粒子不一定属于同种元素 | |
| B. | 两个原子如果核外电子排布相同,一定属于同种元素 | |
| C. | 质子数相同,电子数也相同的两种粒子,不可能是一种分子和一种离子 | |
| D. | 所含质子数和电子数相等的粒子一定是原子 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 4种 | B. | 5种 | C. | 6种 | D. | 7种 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 滴加KI溶液时,KI被氧化,CuI是还原产物 | |
| B. | 通入SO2后,溶液变无色,体现SO2的还原性 | |
| C. | 上述实验条件下,物质的氧化性:Cu2+>I2>SO2 | |
| D. | 整个过程发生了复分解反应和氧化还原反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com