
在复盐NH4Fe(SO4)2溶液中逐滴加入Ba(OH)2溶液,可能发生的反应的离子方程式是
A.Fe2++SO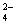 +Ba2++2OH-=BaSO4↓+Fe(OH)2↓
+Ba2++2OH-=BaSO4↓+Fe(OH)2↓
B.NH +Fe3++ 2SO
+Fe3++ 2SO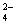 + 2Ba2+
+ 2Ba2+ + 4OH-=2BaSO4↓+ Fe(OH)3↓+ NH3·H2O
+ 4OH-=2BaSO4↓+ Fe(OH)3↓+ NH3·H2O
C.2Fe3++ 3SO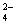 + 3Ba2++6OH-=3BaSO4↓+ 2Fe(OH)3↓
+ 3Ba2++6OH-=3BaSO4↓+ 2Fe(OH)3↓
D.3NH + Fe3++3SO
+ Fe3++3SO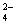 + 3Ba2++ 6OH-=3BaSO4↓+Fe(OH)3↓+3NH3·H2O
+ 3Ba2++ 6OH-=3BaSO4↓+Fe(OH)3↓+3NH3·H2O
 全能测控一本好卷系列答案
全能测控一本好卷系列答案科目:高中化学 来源: 题型:
)如图是某课外活动小组的同学设计的4个喷泉实验方案.下列有关操作不可能引发喷泉现象的是( )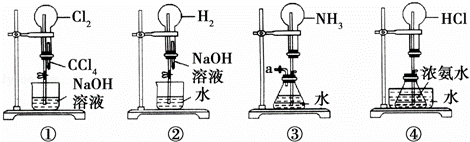
|
| A. | 挤压装置①的胶头滴管使CCl4全部进入烧瓶,片刻后打开止水夹 |
|
| B. | 挤压装置②的胶头滴管使NaOH溶液全部进入烧瓶,片刻后打开止水夹 |
|
| C. | 用鼓气装置从装置③的a处不断鼓入空气并打开止水夹 |
|
| D. | 向装置④的水槽中慢慢加入足量浓硫酸并打开止水夹 |
查看答案和解析>>
科目:高中化学 来源: 题型:
碱式碳酸铜的成分有多种,其化学式一般可表示为xCu(OH)2•yCuCO3.
(1)孔雀石呈绿色,是一种名贵的宝石,其主要成分是Cu(OH)2•CuCO3.某兴趣小组为探究制取孔雀石的最佳反应条件,设计了如下实验:
实验1:将2.0mL 0.50mol•L﹣1的Cu(NO3)2溶液、2.0mL 0.50mol•L﹣1的NaOH溶液和0.25mol•L﹣1的Na2CO3溶液按表Ⅰ所示体积混合.
实验2:将合适比例的混合物在表Ⅱ所示温度下反应.
实验记录如下:
| 编号 | V (Na2CO3)/mL | 沉淀情况 | 编号 | 反应温度/℃ | 沉淀情况 | |
| 1 | 2.8 | 多、蓝色 | 1 | 40 | 多、蓝色 | |
| 2 | 2.4 | 多、蓝色 | 2 | 60 | 少、浅绿色 | |
| 3 | 2.0 | 较多、绿色 | 3 | 75 | 较多、绿色 | |
| 4 | 1.6 | 较少、绿色 | 4 | 80 | 较多、绿色(少量褐色) |
表Ⅰ表Ⅱ
①实验室制取少许孔雀石,应该采用的条件是 n[Cu(NO3)2]:n(Na2CO3)=2:1,75℃ .
②80℃时,所制得的孔雀石有少量褐色物质的原因是 Cu(OH)2受热分解为CuO .
(2)实验小组为测定上述某条件下所制得的碱式碳酸铜样品组成,利用下图所示的装置(夹持仪器省略)进行实验:
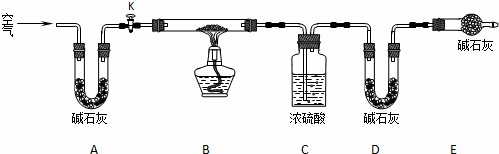
步骤1:检查装置的气密性,将过滤、洗涤并干燥过的样品置于平直玻璃管中.
步骤2:打开活塞K,鼓入空气,一段时间后关闭,称量相关装置的质量.
步骤3:加热装置B直至装置C中无气泡产生.
步骤4: 继续通一段时间空气至装置冷却 .
步骤5:称量相关装置的质量.
①装置A的作用是 除去空气中的CO2和H2O ;若无装置E,则实验测定的x/y的值将 偏小 (选填“偏大”、“偏小”或“无影响”).
②某同学在实验过程中采集了如下数据:
A.反应前玻璃管与样品的质量163.8g
B.反应后玻璃管中残留固体质量56.0g
C.装置C实验后增重9.0g
D.装置D实验后增重8.8g
为测定x/y的值,你认为可以选用上述所采集数据中的 BC、BD、CD (写出所有组合的字母代号)一组即可进行计算,并根据你的计算结果,写出该样品组成的化学式 5Cu(OH)2•2CuCO3 .
查看答案和解析>>
科目:高中化学 来源: 题型:
氮是大气中含量丰富的一种元素,氮及其化合物在生产、生活中有着重要作用,减少氮氧化物的排放是环境保护的重要内容之一.请回答下列氮及其化合物的相关问题:
(1)据报道,意大利科学家获得了极具研究价值的N4,其分子结构与白磷分子的正四面体结构相似.已知断裂1mol N﹣N键吸收167kJ热量,生成1mol N≡N键放出942kJ热量,请写出N4气体转变为N2反应的热化学方程式: N4(g)=2N2(g);△H=﹣882kJ/mol .
(2)据报道,NH3可直接用作车用燃料电池,写出该电池的负极反应式: 2NH3+6OH﹣﹣6e﹣=N2+6H2O .
(3)在T1℃时,将5mol N2O5置于10L固定容积的密闭容器中发生下列反应:2N2O5(g)⇌4NO2(g)+O2(g);△H>0.反应至5分钟时各物质的浓度不再发生变化,测得NO2的体积分数为50%.
①求该反应的平衡常数K=  (数字代入式子即可),上述平衡体系中O2的体积分数为 12.5% .
(数字代入式子即可),上述平衡体系中O2的体积分数为 12.5% .
②用O2表示从0~5min内该反应的平均速率υ(O2)= 0.02mol/(L•min) .
③将上述平衡体系的温度降至T2℃,密闭容器内减小的物理量有 AC .
A.压强 B.密度 C.反应速率 D.N2O5的浓度
(4)在恒温恒容的密闭容器中充入NO2,建立如下平衡:2NO2(g)⇌N2O4(g),平衡时N2O4与NO2的物质的量之比为a,其它条件不变的情况下,分别再充入NO2和再充入N2O4,平衡后引起的变化正确的是 B .
A.都引起a减小
B.都引起a增大
C.充入NO2引起a减小,充入N2O4引起a增大
D.充入NO2引起a增大,充入N2O4引起a减小.
查看答案和解析>>
科目:高中化学 来源: 题型:
在 pH=1的溶液中能大量共存的一组离子或分子是
pH=1的溶液中能大量共存的一组离子或分子是
A.Na+、Mg2+、ClO—、NO B. Al3+、 NH
B. Al3+、 NH 、 Br- 、Cl-
、 Br- 、Cl-
C.K+ 、Cr2O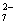 、CH3CHO、 SO
、CH3CHO、 SO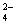 D.Na+、K+ 、SiO
D.Na+、K+ 、SiO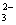 、Cl-
、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液X中只可能溶有K+、Mg2+、Al3+、AlO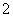 、SiO
、SiO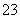 、SO
、SO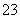 、CO
、CO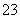 、SO
、SO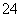 中的若干种离子。某同学对该溶液进行了如下实验:
中的若干种离子。某同学对该溶液进行了如下实验:
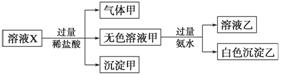
下列判断正确的是 ( )
A.气体甲一定是纯净物
B.沉淀甲是硅酸和硅酸镁的混合物
C.K+、AlO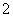 和SiO
和SiO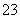 一定存在于溶液X中
一定存在于溶液X中
D.CO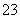 和SO
和SO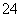 一定不存在于溶液X中
一定不存在于溶液X中
查看答案和解析>>
科目:高中化学 来源: 题型:
下列对应化学反应的离子方程式正确的是
A.氨水中通入过量SO2:SO2+NH3·H2O===NH +HSO
+HSO
B.(CH3COO)2Ba溶液中加入稀硫酸:Ba2++SO ===BaSO4↓
===BaSO4↓
C.用铜作电极电解CuSO4溶液:2Cu2++2H2O 2Cu↓+O2↑+4H+
2Cu↓+O2↑+4H+
D.Al2(SO4)3溶液中加入足量Ba(OH)2溶液:Al3++2SO +2Ba2++4OH-===2BaSO4↓+AlO
+2Ba2++4OH-===2BaSO4↓+AlO +2H2O
+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
某工厂排出的污水中含有大量的Fe2+、Zn2+、Hg2+三种金属离子。以下是某化学研究性学习小组的同学设计除去污水中的金属离子,并回收绿矾、皓矾(ZnSO4·7H2O)和汞的方案。
【药品】 NaOH溶液、硫化钠溶液、硫化亚铁、稀硫酸、铁粉
【实验方案】

【问题探究】
(1)步骤Ⅱ所发生反应的离子方程式为__________________________________。
(2)步骤Ⅲ中抽滤的目的是____________,该步骤产生Fe(OH)3的反应的离子方程式为
________________________________________________________________________。
(3)步骤Ⅵ中得到硫酸锌溶液的离子方程式为_________________________________________。
(4)欲实现步骤Ⅴ,需加入的试剂有________、________,所涉及的主要操作依次为_____________。
(5)步骤Ⅳ常用的方法是________,该步骤是否对环境有影响?________(填“是”或“否”),如有影响,请你设计一个绿色环保方案来实现步骤Ⅳ的反应:__________。
(6)该研究小组的同学在强碱溶液中,用次氯酸钠与Fe(OH)3反应获得了高效净水剂Na2FeO4,该反应的离子方程式为_______________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,氯元素被氧化的是( )
A.2KClO3 2KCl+3O2↑
2KCl+3O2↑
B.2P+5Cl2===2PCl5
C.MnO2+4HCl(浓) MnCl2+2H2O+Cl2↑
MnCl2+2H2O+Cl2↑
D.H2+Cl2===2HCl
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com