
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g•cm-3 | 溶解性 |
| 乙二醇( C2H6O2) | -11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、酒精以任意比互溶 |

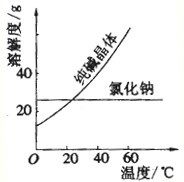
分析 (1)由图可知,氯化钠、纯碱的溶解度受温度影响不同;
(2)由表格中数据可知,乙二醇和丙三醇互溶,但沸点不同;
(3)蒸馏是利用物质的沸点不同分离相互溶解的沸点不同的液体,蒸馏时用到蒸馏烧瓶、酒精灯、冷凝管、牛角管、锥形瓶等仪器,注意温度计水银球应处在蒸馏烧瓶的支管口附近,冷凝管应从下口进水,上口出水,以保证水充满冷凝管,起到充分冷凝的作用,为防止溶液爆沸,应加入少量碎瓷片;水浴加热优点:使蒸馏烧瓶受热均匀,便于控制温度.
解答 解:(1)由图可知,氯化钠、纯碱的溶解度受温度影响不同,则将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用“溶解、结晶、过滤”的方法,
故答案为:C;
(2)由表格中数据可知,乙二醇和丙三醇互溶,但沸点不同,则分离的最佳方法是蒸馏法,
故答案为:A;
(3)①蒸馏实验中,温度计测量的是蒸汽的温度所以,温度计下端的水银球不能插入溶液中,温度计的水银球在蒸馏瓶的支管口处;
②为到达最佳冷凝效果,冷凝水应下进上出;
③烧杯加热应垫上石棉网;
因有机溶剂为CCl4(沸点为77℃),低于水的沸点,所以选择水浴加热使蒸馏烧瓶受热均匀,便于控制温度;
故答案为:温度计下端的水银球不能插入溶液中;冷凝管进出水的方向颠倒;加热烧杯未垫上石棉网;受热均匀,便于控制温度.
点评 本题考查混合物分离提纯的实验设计,为高频考点,把握习题中的信息、混合物分离提纯实验、实验操作及技能为解答的关键,侧重分析与实验能力的考查,注意图象及表格数据的应用,题目难度不大.


 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:选择题
| A. | 干冰用于人工降雨 | |
| B. | 蔗糖中加入浓硫酸,蔗糖变黑,体积膨胀 | |
| C. | 溶洞中钟乳石的形成 | |
| D. | 豆科作物的根瘤菌对空气中氮的固定 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
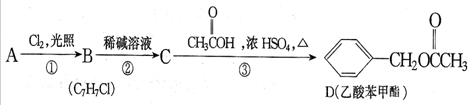
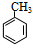 .
.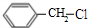 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$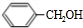 +NaCl.
+NaCl.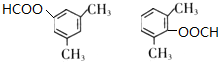 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 族 周期 | IA | IIA | IIIA | IVA | VA | VIA | VIIA | 0 |
| 2 | ⑥ | |||||||
| 3 | ① | ③ | ⑤ | ⑦ | ⑧ | ⑩ | ||
| 4 | ② | ④ | ⑨ |
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
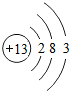 ,其最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
,其最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O. ,其中一种氢化物在常温下与MnO2混合的反应化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
,其中一种氢化物在常温下与MnO2混合的反应化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑. ,高温灼伤该化合物时,火焰呈黄色.
,高温灼伤该化合物时,火焰呈黄色.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 石油裂解主要目的是得到短链的不饱和烃 | |
| B. | 煤中含有苯和甲苯,可用先干馏后分馏的方法将它们分离出来 | |
| C. | 煤的气化与液化都是化学变化 | |
| D. | 含C18以上烷烃的重油经过催化裂化可以得到汽油 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com