
实验室中以下物质的贮存方法不正确的是( )
A.浓硝酸用带橡胶塞的细口、棕色试剂瓶盛放,并贮存在阴凉处
B.少量金属钠保存在煤油中
C.少量液溴可用水封存,防止溴挥发
D.保存硫酸亚铁溶液时,要向其中加入少量硫酸和铁粉
科目:高中化学 来源: 题型:
用CH4催化还原NOx可以消除氮氧化物的污染。已知CH4(g)+4NO2(g)===4NO(g)+CO2(g)+2H2O(g) ΔH=-574 kJ·mol-1,CH4(g)+4NO(g)===2N2(g)+CO2(g)+2H2O(g) ΔH=-1 160 kJ·mol-1。若在标准状况下4.48 L CH4恰好能将一定量NO2还原成N2和H2O(g),则整个过程中放出的热量为( )
A.114.8 kJ B.232 kJ
C.368.8 kJ D.173.4 kJ
查看答案和解析>>
科目:高中化学 来源: 题型:
①CaCO3(s)===CaO+CO2(g) ΔH=177.7 kJ
②C(s)+H2O(s)===CO(g)+H2(g)
ΔH=-131.3 kJ/mol
③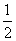 H2SO4(l)+NaOH(l)===
H2SO4(l)+NaOH(l)===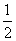 Na2SO4(l)+H2O(l)
Na2SO4(l)+H2O(l)
ΔH=-57.3 kJ/mol
④C(s)+O2(g)===CO2(g) ΔH=-393.5 kJ/mol
⑤CO(g)+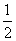 O2(g)===CO2(g) ΔH=-283 kJ/mol
O2(g)===CO2(g) ΔH=-283 kJ/mol
⑥HNO3(aq)+NaOH(aq)===NaNO3(aq)+H2O(l)
ΔH=-57.3 kJ/mol
⑦2H2(g)+O2(g)===2H2O(l) ΔH=-517.6 kJ/mol
(1)上述热化学方程式中,不正确的有________,不正确的理由分别是_______________________________________________________________。
(2)根据上述信息,写出C转化为CO的热化学方程式_____________。
(3)上述反应中,表示燃烧热的热化学方程式有________________;表示中和热的热化学方程式有________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
将a g铁和氧化铁的混合物加入足量的盐酸中充分反应后,固体无剩余,测得参加反应的HCl为0.08 mol,放出标准状况下气体0.224 L.则下列判断中正确的是
A.原混合物中n(Fe)∶n(Fe2O3)=2∶1
B.向溶液中滴入KSCN溶液,显红色
C.无法计算原混合物的质量a
D.此时溶液中Fe2+和Fe3+的物质的量之比为3∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
关于物质的分类正确的是( )
A.SO2、CO2、CO、NO2都是酸性氧化物
B.Na2O、Na2O2、Fe2O3、CuO都是碱性氧化物
C.HCl、HClO、HNO3、HClO4都是强酸
D.NaOH、KOH、Ba(OH)2、Ca(OH)2都是强碱
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学弄清楚喷泉实验的原理后,有了一个创新的想法,如果改换一下烧瓶内的气体,以及胶头滴管和烧杯内的液体,也应该可以做喷泉实验。他用课本上所用的装置实际做了一下,果真得到了美丽的喷泉。下列组合中不可能是该同学设计的组合的是( )
A.氯化氢和水 B.氧气和水 C.二氧化碳和NaOH溶液 D.氯气和NaOH溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
下列的离子方程式中,书写正确的一项是( )
A.氨水中通入过量CO2:2NH3·H2O +CO2==== 2NH4++CO32-+H2O
B.稀硝酸中加入过量铁粉:3Fe + 8H++2 NO3-==== 3Fe2++ 2NO↑ + 4H2O
C.钠与水反应 Na+2H2O==== Na+ +2OH-+H2 ↑
D.Ca(ClO)2 溶液中通入过量的二氧化硫气体:ClO-+SO2+H2O==== HClO+HSO3-
查看答案和解析>>
科目:高中化学 来源: 题型:
盖斯定律认为能量总是守恒的,不管化学反应过程是一步完成或分几步完成,整个过程的热效应是相同的。已知:
①H2O(g)====H2O(l) ΔH1=-Q1kJ·mol-1
②C2H5OH(g)====C2H5OH(l) ΔH2=-Q2kJ·mol-1
③C2H5OH(g)+3O2(g)====2CO2(g)+3H2O(g) ΔH3=- Q3kJ·mol-1
若使23 g液态无水酒精完全燃烧,最后恢复到室温,则放出的热量为(单位:kJ)( )
A.Q1+ Q2+ Q3 B.1.5Q1-0.5Q2+0.5Q3
C.0.5Q1-1.5Q2+0.5Q3 D.0.5(Q1+Q2+Q3)
查看答案和解析>>
科目:高中化学 来源: 题型:
下表是部分短周期元素的原子半径及主要化合价,以下叙述正确的是( )
| 元素代号 | L | M | Q | R | T |
| 原子半径 | 0.160 nm | 0.143 nm | 0.112 nm | 0.104 nm | 0.066 nm |
| 主要化合价 | +2 | +3 | +2 | +6、-2 |
|
A.气态氢化物的稳定性为H2T<H2R
B.单质与稀盐酸反应的速率为L<Q
C.M与T形成的化合物具有两性
D.L2+与R2-的核外电子数相等
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com