
利用LiOH和钴氧化物可制备锂离子电池正极材料。LiOH可由电解法制备,钴氧化物可通过处理钴渣获得。
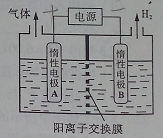
(1)利用如图装置电解制备LiOH,两电极区电解液分别为LiOH和LiCl溶液。B极区电解液为__________溶液(填化学式),阳极电极反应式为__________ ,电解过程中Li+向_____电极迁移(填“A”或“B”)。
(2)利用钴渣[含Co(OH)3、Fe(OH)3等]制备钴氧化物的工艺流程如下:
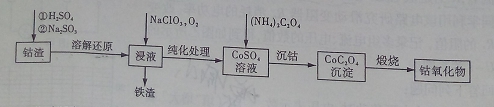
Co(OH)3溶解还原反应的离子方程式为____________________________________,铁渣中铁元素的化合价为___________,在空气中煅烧CoC2O4生成钴氧化物和CO2,测得充分煅烧后固体质量为2.41g,CO2的体积为1.344L(标准状况),则钴氧化物的化学式为__________。
【答案】(1)LiOH;2Cl--2e-=Cl2↑;B
(2)2Co(OH)3+4H++SO32-=2Co2++SO42-+5H2O;+3;Co3O4
【解析】(1)B极区由H+得到电子生成H2,同时生成LiOH,则B极区电解液为LiOH溶液;电极A为阳极,阳极区电解液为LiCl溶液,根据放电顺序,阳极上Cl-失去电子,则阳极电极反应式为:2Cl--2e-=Cl2↑;在电解池中,阳离子向阴极移动,故电解过程中Li+向B电极迁移。
(2)在酸性条件下,Co(OH)3首先与H+反应生成Co3+,Co3+具有氧化性,把SO32-氧化为SO42-,配平可得离子方程式:2Co(OH)3+4H++SO32-=2Co2++SO42-+5H2O;氯酸钠和臭氧具有氧化性,可将二价铁氧化为三价铁,故铁渣中铁元素的化合价应该为+3价;CO2的物质的量为:1.344L÷22.4L/mol=0.06mol,根据CoC2O4的组成可知Co元素物质的量为0.03mol,设钴氧化物的化学式为CoxOy,根据元素的质量比可得:59x∶16y=(0.03mol×59g/mol)∶(2.41g-0.03mol×59g/mol),解得x∶y=3∶4,则钴氧化物的化学式为:Co3O4。


 名校练考卷期末冲刺卷系列答案
名校练考卷期末冲刺卷系列答案科目:高中化学 来源: 题型:
实验室制备下列气体时,所用方法正确的是( )
A.制氧气时,用Na2O2或H2O2作反应物可选择相同的气体发生装置
B.制氯气时,用饱和NaHCO3溶液和浓硫酸净化气体
C.制乙烯时,用排水法或向上排空气法收集气体
D.制二氧化氮时,用水或NaOH溶液吸收尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
不能作为判断硫、氯两种元素非金属性强弱的依据是( )
A.单质氧化性的强弱 B.单质沸点的高低
C.单质与氢气化合的难易 D.最高价氧化物对应的水化物酸性的强弱
查看答案和解析>>
科目:高中化学 来源: 题型:
酸性锌锰干电池是一种一次性电池,外壳为金属锌,中间是碳棒,其周围是有碳粉、MnO2、ZnCl2和NH4Cl等组成的糊状填充物。该电池放电过程产生MnOOH。回收处理该废电池可得到多种化工原料。有关数据如下表
溶解度/(g/100g水)
|
化合物 | 0 | 20 | 40 | 60 | 80 | 100 |
| NH4Cl | 29.3 | 37.2 | 45.8 | 55.3 | 65.6 | 77.3 |
| ZnCl2 | 343 | 395 | 452 | 488 | 541 | 614 |
| 化合物 | Zn(OH)2 | Fe(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-17 | 10-17 | 10-39 |
回答下列问题:
(1)该电池的正极反应式为________,电池反应的离子方程式为________。
(2)维持电流强度为0.5
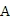 ,电池工作5分钟,理论上消耗锌________
,电池工作5分钟,理论上消耗锌________
 。(已知
。(已知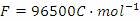
 )
)
(3)废电池糊状填充物加水处理后,过滤,滤液中主要有
 ,二者可通过_____分离回收;滤渣的主要成分是
,二者可通过_____分离回收;滤渣的主要成分是
 、_______和_______,欲从中得到较纯的
、_______和_______,欲从中得到较纯的
 ,最简便的方法为_________,其原理是_________。
,最简便的方法为_________,其原理是_________。
(4)用废电池的锌皮制备
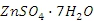 的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀
的过程中,需除去锌皮中的少量杂质铁,其方法是:加稀
 溶解,铁变为______,加碱调节至pH为_______时,铁刚好沉淀完全(离子浓度小于
溶解,铁变为______,加碱调节至pH为_______时,铁刚好沉淀完全(离子浓度小于
 时,即可认为该离子沉淀完全);继续加碱至pH为_____时,锌开始沉淀(假定
时,即可认为该离子沉淀完全);继续加碱至pH为_____时,锌开始沉淀(假定
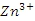 浓度为0.1mol
浓度为0.1mol
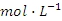 )。若上述过程不加
)。若上述过程不加
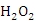 后果是______,原因是_______.
后果是______,原因是_______.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应中,反应后固体物质增重的是( )
A.氢气通过灼热的CuO粉末
B.二氧化碳通过Na2O2粉末
C.铝与Fe2O3发生铝热反应
D.将锌粒投入Cu(NO3)2溶液
查看答案和解析>>
科目:高中化学 来源: 题型:
能正确表示下列反应的离子方程式的是( )
A.Cl2通入NaOH溶液:
Cl2+OH-===Cl-+ClO-+H2O
B.NaHCO3溶液中加入稀盐酸:
CO +2H+===CO2↑+H2O
+2H+===CO2↑+H2O
C.AlCl3溶液中加入过量稀氨水:
Al3++4NH3·H2O===AlO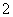 +4NH
+4NH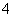 +2H2O
+2H2O
D.Cu溶于稀HNO3:
3Cu+8H++2NO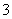 ===3Cu2++2NO↑+4H2O
===3Cu2++2NO↑+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,下列各组物质中,Y既能与X反应又能与Z反应的是( )
| X | Y | Z | |
| ① | NaOH溶液 | Al(OH)3 | 稀硫酸 |
| ② | KOH溶液 | SiO2 | 浓盐酸 |
| ③ | O2 | N2 | H2 |
| ④ | FeCl3溶液 | Cu | 浓硝酸 |
A.①③ B.①④ C.②④ D.②③
查看答案和解析>>
科目:高中化学 来源: 题型:
实脸室采用MgCl2、AlCl3的混合溶液与过量氨水反应制备MgAl2O4二主要流程如下:


(1)为使Mg2+、Al3+同时生成沉淀,应先向沉淀反应器中加入 (填“A”或“B"),再滴加另一反应物。
(2)如右图所示,过滤操作中的一处错误是 。
(3)判断流程中沉淀是否洗净所用的试剂是 。高温焙烧时,用于盛放固体的仪器名称是 。
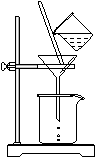

(4)无水AlCl3(183℃升华)遇潮湿空气即产生大量白雾,实验室可用下列装置制备。


装置B中盛放饱和NaCl溶液,该装置的主要作用是 。F中试剂的作用是 。用一件仪器装填适当试剂后也可起到F和G的作用,所装填的试剂为 _。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com