
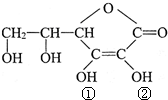
 维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,结构如图,下列关于维生素C正确的是( )
维生素C(VitaminC)又名抗坏血酸,具有酸性和强还原性,也是一种常见的食品添加剂,结构如图,下列关于维生素C正确的是( )| A、维生素C能使酸性高锰酸钾溶液褪色 |
| B、维生素C由于含有酯基而难溶于水 |
| C、维生素C酸性可能是①②两个羟基引起的 |
| D、维生素C由于含有C=O键而能发生银镜反应 |


科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、ICN不能和NaOH溶液反应 |
| B、ICN是一种共价化合物 |
| C、将ICN加入到氯水中可生成I2 |
| D、ICN的晶体是离子晶体 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、向漂白液中通入过量CO2:ClO-+H2O+CO2═HClO+HCO3- |
| B、将磁性氧化铁溶于盐酸:Fe3O4+8H+═3Fe3++4H2O |
| C、氯气与水反应:Cl2+H2O═2H++Cl-+ClO- |
| D、将铁粉加入稀硫酸中:2Fe+6H+═2Fe3++3H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图是一燃料电池的化学原理示意图,该燃料电池总反应化学方程式为:2CH3OH+3O2+4KOH
如图是一燃料电池的化学原理示意图,该燃料电池总反应化学方程式为:2CH3OH+3O2+4KOH| 放电 |
| 充电 |
| A、电极A为电池负极 |
| B、电极B表面上发生还原反应 |
| C、工作一段时间溶液pH保持不变 |
| D、燃料电池工作时不会出现火焰 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化合物与混合物属于并列关系 |
| B、氢化物与氧化物属于交叉关系 |
| C、强电解质与酸属于包含关系 |
| D、氧化还原反应与置换反应属于交叉关系 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Ba(OH)2溶液和H2SO4溶液混合 |
| B、NaOH溶液和盐酸混合 |
| C、Cu(OH)2和稀H2SO4反应 |
| D、CO2通入NaOH溶液中 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、X和Y可能位于同一周期或相邻周期 |
| B、X和Y可能位于同一主族或相邻主族 |
| C、X和Y可能形成离子晶体XY |
| D、X和Y可能形成原子晶体XY2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、化学平衡常数是指一定条件下的可逆反应,生成物浓度的幂之积与反应物浓度的幂之积的比值 |
| B、已知4HCl(g)+O2(g)═2H2O(g)+2Cl2(g) 能自发进行,则该反应△H<0,△S>0 |
| C、其他条件不变,增大压强,平衡可能移动,但平衡常数一定不变 |
| D、铁制品表面镶锌块和铁制品表面镀锡,都能起到防腐的作用且防腐原理是相同的 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com