
四种短周期元素在周期表中的位置如下图,其中只有M为金属元素。下列说法不正确的是( )

A. 原子半径Z < M
B. Y的最高价氧化物对应水化物的酸性比X 的弱
C. X 的最简单气态氢化物的热稳定性比Z的小
D. Z位于元素周期表中第二周期第ⅥA族
 世纪百通主体课堂小学课时同步达标系列答案
世纪百通主体课堂小学课时同步达标系列答案 世纪百通优练测系列答案
世纪百通优练测系列答案 百分学生作业本题练王系列答案
百分学生作业本题练王系列答案科目:高中化学 来源:2016-2017学年河北省石家庄市高一上学期期末考试化学试卷(解析版) 题型:实验题
为验证浓硫酸与木炭粉在加热条件下反应产生的所有气体产物,设计如下实验:
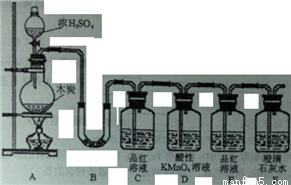
(1)写出浓硫酸与木炭粉反应的化学方程式_____________。
(2)B中加入的试剂是_____,现象是______;C的作用是____,E的作用是________。
(3)如果将F放在B、C之间,则一定不能检出的物质是_______。
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高一上学期期末考试化学试卷(解析版) 题型:选择题
向盛有Cl2的三个集气瓶甲、乙、丙中各注入下列液体中的一种,经过振荡,现象如下图所示,则甲、乙、丙中注入的液体分别是
①AgNO3溶液 ②NaOH溶液 ③水
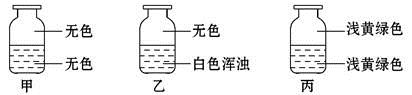
A. ①②③ B. ②①③ C. ③②① D. ①③②
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三上学期期末联考化学试卷(解析版) 题型:简答题
化学在解决雾霾污染中有着重要的作用,雾霾由多种污染物形成,其中包含颗粒物PM2.5)、
氮氧化物(NOx)、CO、SO2等.
(1)已知:NO(g)+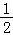 O2(g)═NO2(g)△H=﹣56.5kJ•mol﹣1
O2(g)═NO2(g)△H=﹣56.5kJ•mol﹣1
2SO2(g)+O2(g)═2SO3(g)△H=﹣196.6kJ•mol﹣1
则反应NO2(g)+SO2(g)═SO3(g)+NO(g)△H=_________kJ•mol﹣1.
一定条件下,将NO2与SO2以物质的量比1:2置于恒温恒容的密闭容器中发生上述反应,
下列能说明反应达到平衡状态的有____________
a.混合气体的平均相对分子质量
b.混合气体颜色保持不变
c.SO3和NO的体积比保持不变
d.每消耗1mol SO3的同时生成1mol NO2
测得上述反应平衡时NO2与SO2物质的量比为1:3,则平衡常数K=________(用分数表示)
NH3催化还原氮氧化物(SCR)技术是目前应用最广泛的烟气氮氧化物脱除技术。在氨气足量的情况下,不同c(NO2)/c(NO),不同温度对脱氮率的影响如图所示(已知氨气催化还原氮氧化物的正反应为放热反应),请解释300℃之后脱氮率逐渐减小的原因:__________________________
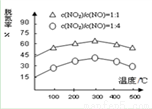
(2)CO综合利用.
①CO用于合成甲醇反应方程式为:CO(g)+2H2(g)═CH3OH(g)
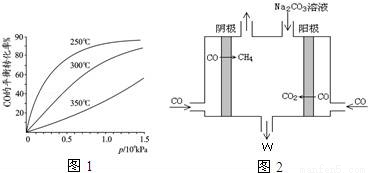
若起始投入1molCO,2mol H2,CO在不同温度下的平衡转化率与压强的关系如图所示.得知该反应的△H_________0,该反应的实际生产条件控制在 250 ℃、1.3×104kPa左右最为适宜.反应达平衡后,下列操作既能加快反应速率,又能使平衡混合物中CH3OH物质的量分数增大的是____________
a. 升温 b.恒容条件下充入H2
c.加入合适的正催化剂 d.恒容条件下再充入1molCO,2mol H2
e.压缩体积 f.移走一部分CH3OH
②电解CO制备CH4,电解质为碳酸钠溶液,工作原理如图2所示,写出阴极区电极
反应式_______________
(3)利用喷雾干燥法脱硫工艺是除去SO2的常见方法,先将含SO2的废气溶于水,再用饱和石灰浆吸收,具体步骤如下:
SO2(g)+H2O(l)  H2SO3(l)
H2SO3(l)  H+(aq)+HSO
H+(aq)+HSO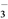 (aq) Ⅰ
(aq) Ⅰ
HSO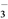 (aq)
(aq)  H+(aq)+SO
H+(aq)+SO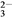 (aq) Ⅱ
(aq) Ⅱ
Ca(OH)2(s)  Ca2+(aq)+2OH-(aq) Ⅲ
Ca2+(aq)+2OH-(aq) Ⅲ
Ca2+(aq)+SO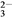 (aq)
(aq)  CaSO3(s) Ⅳ
CaSO3(s) Ⅳ
该温度下,测定吸收后液体中c(Ca2+)一直保持为0.70 mol/L,已知Ksp(CaSO3)=1.4×10-7,则吸收后溶液中的SO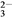 的浓度为_________________
的浓度为_________________
查看答案和解析>>
科目:高中化学 来源:2017届福建省漳州市八校高三上学期期末联考化学试卷(解析版) 题型:选择题
燃料电池具有能量转化率高、无污染等特点,下图为Mg-NaClO燃料电池结构示意图,下列说法正确的是( )
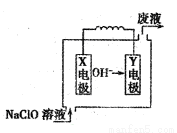
A. 镁作Y电极
B. 电池工作时,Na+向负极移动
C. 废液的pH大于NaClO溶液的pH
D. X电极上发生的反应为ClO-+2H2O - 4e-═ClO3-+4H+
查看答案和解析>>
科目:高中化学 来源:2016-2017学年广东省高二上学期期末考试化学(理)试卷(解析版) 题型:简答题
冬季是雾霾天气高发的季节,其中汽车尾气和燃煤尾气是造成雾霾的原因之一。
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)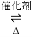 2CO2(g)+N2(g)
2CO2(g)+N2(g)
①在一定条件下,在一个容积固定为2L的密闭容器中充入0.8molNO和1.20molCO,开始反应至3min时测得CO的转化率为20%,则用N2表示的平均反应速率为V(N2)=__________。
②对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(CB)也可以表示平衡常数(记作Kp),则该反应平衡常数的表达式Kp=______________。
③该反应在低温下能自发进行,该反应的△H_______0,(选填“>”、“=”或“<”)
④在某一绝热,恒容的密闭容器中充入一定量的NO、CO发生上述反应,测得正反应的速率随时间变化的曲线如图所示(已知t2—t1=t3—t2)。则下列说法不正确的是__________。(填编号)
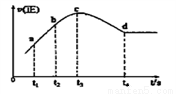
A.反应在c点未达到平衡状态 B.反应速率a点小于b点
C.反应物浓度a点大于b点 D.NO的转化率t1—t2=t2—t3
(2)使用甲醇汽油可能减少汽车尾气对环境的污染,某化工厂用水煤气为原料合成甲醇,恒温条件下,在体积可变的密闭容器中发生反应:CO(g)+2H2(g)?CH3OH(g),到达平衡时,测得CO、H2、CH3OH分别为1mol、1mol、1mol,容器的体积为3L,现往容器中继续通人3mol CO,此时v(正)____v(逆)(选填‘‘>”、“<’’或“=”),判断的理由____________。
(3)二甲醚也是清洁能源,用合成气在催化剂存在下制备二甲醚的反应原理为:
2CO(g)+4H2(g)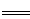 CH3OCH3(g)+H2O(g)
CH3OCH3(g)+H2O(g)
已知一定条件下,该反应中CO的平衡转化率随温度、投料比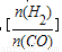 的变化曲线如图:
的变化曲线如图:
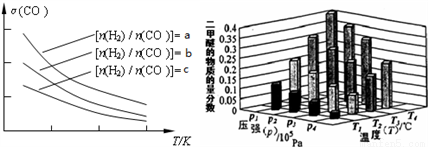
①a、b、c按从大到小的顺序排序为___________。
②某温度下,将2.0mol CO(g)和4.0mol H2(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如上图所示,关于温度和压强的关系判断正确的是___________;
A.P3>P2,T3>T2 B.P1>P3,T1>T3
C.P2>P4,T4>T2 D.P1>P4,T2>T3
③在恒容密闭容器里按体积比为1:2充入一氧化碳和氢气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是___________:
A.正反应速率先增大后减小
B.逆反应速率先增大后减小
C.化学平衡常数K值增大
D.反应物的体积百分含量增大
E.混合气体的密度减小
F.氢气的转化率减小
查看答案和解析>>
科目:高中化学 来源:2016-2017学年山东省高二下学期开学考试化学试卷(解析版) 题型:选择题
为比较Fe3+和Cu2+对H2O2分解反应的催化效果,甲乙两组同学分别设计了如图1、图2所示的实验。下列叙述中不正确的是
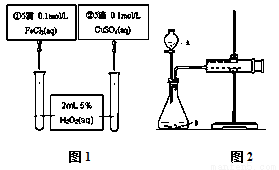
A. 图1实验可通过观察产生气泡快慢来比较反应速率的大小
B. 若图1所示实验中反应速率为①>②, 则一定说明Fe3+比Cu2+对H2O2分解催化效果好
C. 用图2装置测定反应速率,可测定反应产生的气体体积及反应时间
D. 为检查图2装置的气密性,可关闭A处活塞,将注射器活塞拉出一定距离,一段时间后松开活塞,观察活塞是否回到原位
查看答案和解析>>
科目:高中化学 来源:2016-2017学年湖北省宜昌市高二上学期期末考试化学试卷(解析版) 题型:简答题
研究CO2的利用对促进低碳社会的构建具有重要意义。
(1)将CO2与焦炭作用生成CO,CO可用于炼铁等。
已知:Fe2O3(s)+3C(s,石墨)=2Fe(s)+3CO(g)Δ H1=+489.0 kJ·mol-1
C(s,石墨)+CO2(g)=2CO(g) ΔH 2=+172.5 kJ·mol-1
则CO还原Fe2O3(s)的热化学方程式为________________。
(2)二氧化碳合成甲醇是碳减排的新方向,将CO2转化为甲醇的热化学方程式为:
CO2(g)+3H2(g) CH3OH(g)+H2O(g) ΔH
CH3OH(g)+H2O(g) ΔH
①取一定体积CO2和H2的混合气体(物质的量之比为1∶3),加入恒容密闭容器中,发生上述反应反应过程中测得甲醇的体积分数φ(CH3OH)与反应温度T的关系如图1所示,则该反应的
ΔH____________0(填“>”、“<”或“=”,下同)。
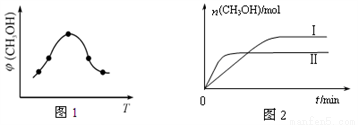
②在两种不同条件下发生反应,测得CH3OH的物质的量随时间变化如图2所示,曲线I、Ⅱ对应的平衡常数关系为KⅠ____________KⅡ。
(3)以CO2为原料还可以合成多种物质。
①工业上尿素[CO(NH2)2]由CO2和NH3在一定条件下合成。开始以氨碳比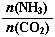 =3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为_______________。
=3进行反应,达平衡时CO2的转化率为60%,则NH3的平衡转化率为_______________。
②将足量CO2通入饱和氨水中可得氮肥NH4HCO3,已知常温下一水合氨Kb=1.8×10-5,碳酸一级电离常数Ka=4.3×10-7,则NH4HCO3溶液呈_______________(填“酸性”、“中性”或“碱性”)。
查看答案和解析>>
科目:高中化学 来源:2017届河北省高三上学期期末考试理综化学试卷(解析版) 题型:选择题
化学与生产生活密切相关,下列物质的用途及解释均正确的是
选项 | 用途 | 解释 |
A | 可用FeCl3溶液刻蚀铜制电路板 | Fe3+的氧化性强于Cu2+ |
B | 碳与石英反应可冶炼粗硅 | 碳的非金属性比硅强 |
C | 四氯化碳可用于灭火 | 四氯化碳的沸点高 |
D | 酸性KMnO4溶 液可漂白织物 | KMnO4有强氧化性 |
A. A B. B C. C D. D
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com