
 ��ҵ��ͨ���ù�ҵ�ƾ�����ʯ�һ��������ȡ��ˮ�Ҵ�����ͼ��ʵ������ģ�ҵԭ����ȡ��ˮ�Ҵ���װ�ã�
��ҵ��ͨ���ù�ҵ�ƾ�����ʯ�һ��������ȡ��ˮ�Ҵ�����ͼ��ʵ������ģ�ҵԭ����ȡ��ˮ�Ҵ���װ�ã����� ��1����ϸ�۲���ȡ��ˮ�Ҵ���װ��ͼ����֪����ƿ����δ��ʯ�������¶ȼƵ�ˮ����Ӧ������Һ�У���ȴˮ�ķ���ӷ��ˣ�
��2�������������ʯ�Һ��γɵ��Ҵ���Ca��OH��2�����Һ���ֲ㣬�����÷�Һ�ķ������룻
��3����ʯ����ˮ��Ӧ�����Գ�ȥ��ҵ�ƾ��е�ˮ��CaO+H2O�TCa��OH��2��
��4����װ��ͼ��֪������A���¶ȼƣ�����B��������ƿ������C�������ܣ�
��5������������У�����B�м����ʯ�������Ƭ�������Է�ֹ���У�
��� �⣺��1����ϸ�۲���ȡ��ˮ�Ҵ���װ��ͼ����֪����ƿ����δ��ʯ�������¶ȼƵ�ˮ����Ӧ������Һ�У���ȴˮ�ķ���ӷ��ˣ�
�ʴ�Ϊ������ƿ����δ��ʯ�������¶ȼƵ�ˮ���������Һ�У���ȴˮ�ķ���ӷ��ˣ�
��2�������������ʯ�Һ��γɵ��Ҵ���Ca��OH��2�����Һ���ֲ㣬�����÷�Һ�ķ������룬
�ʴ�Ϊ��C��
��3����ʯ����ˮ��Ӧ�����Գ�ȥ��ҵ�ƾ��е�ˮ��CaO+H2O�TCa��OH��2��
�ʴ�Ϊ��CaO+H2O�TCa��OH��2��
��4����װ��ͼ��֪������C�������ܣ�
�ʴ�Ϊ�������ܣ�
��5������������У�����B�м����ʯ�������Ƭ�������Է�ֹ���У�
�ʴ�Ϊ����ֹ���У�
���� ���⿼���л�������ʼ�ʵ�飬�漰֪ʶ��϶࣬�ۺ���ǿ���ϺõĿ���ѧ����������������������Ŀ�Ѷ��еȣ�



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ����ʽΪC7H8O���б��������ڴ����ͬ���칹����4�� | |
| B�� | ��Ȳ��ʹ������Ȼ�̼��Һ��ɫ�Ƿ�����������Ӧ | |
| C�� | ������������ԭ�Ӷ���ͬһƽ���� | |
| D�� | �������������������ʿɼӱ���NaOH��Һ��Һ��ȥ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 32 g�������������������У���������ԭ����Ϊ2��6.02��1023 | |
| B�� | ��״���£�11.2 L���Ȼ�̼���еķ�����Ϊ0.5��602��1023 | |
| C�� | 5.6 g������ȫ�������ᣬʧȥ�ĵ�����һ��Ϊ0.3��6.02��1023 | |
| D�� | 1 L0.5 mol/L Na2CO3 ��Һ�к��е�CO32-��ĿΪ0.5��6.02��1023 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��״���£�11.2LCCl4���еķ�����ĿΪ0.5NA | |
| B�� | ��10mL 1 mol/L FeCl3���˵����ˮ�У�������������������Ϊ0.01NA | |
| C�� | 1 mol/LNa2O2�����к���������Ϊ3NA | |
| D�� | 0.1moIH2O��D2O��ɵĻ�����к�����������NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
| ʵ���� | �� | �� | �� | �� | �� |
| �¶ȣ��棩 | 30 | 40 | 50 | 60 | 70 |
| ��ɫʱ�䣨s�� | 160 | 80 | 40 | 20 | 10 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
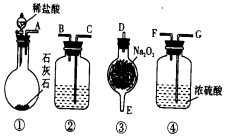 ʵ��������ͼ��ʾ������ҩƷ��CO2��Na2O2��Ӧ��O2��ʵ�飬����д���пհף�
ʵ��������ͼ��ʾ������ҩƷ��CO2��Na2O2��Ӧ��O2��ʵ�飬����д���пհף��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
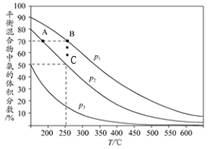 ���ڹ�����ռ����Ҫ��λ��
���ڹ�����ռ����Ҫ��λ���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com