
| A. | 植物油是高分子化合物 | |
| B. | 淀粉水解的最终产物是葡萄糖 | |
| C. | 葡萄糖能发生水解和氧化反应 | |
| D. | 蛋白质溶液遇硫酸铜后产生的沉淀能重新溶于水 |
分析 A.相对分子质量在10000以上的有机化合物为高分子化合物;
B.淀粉在酸的催化作用下,水解生成麦芽糖,麦芽糖水解生成葡萄糖;
C.葡萄糖能发生氧化反应,但不能发生水解反应;
D.硫酸铜为重金属盐,使蛋白质发生变性,变性为不可逆过程.
解答 解:A.植物油属于油脂是小分子有机化合物,故A错误;
B.淀粉为多糖,水解生成麦芽糖,麦芽糖水解生成葡萄糖,所以淀粉水解的最终产物是葡萄糖,故B正确;
C.葡萄糖为五羟基醛,含有羟基、醛基,能发生氧化反应,但葡萄糖为单糖,不能发生水解反应,故C错误;
D.硫酸铜为重金属盐,使蛋白质发生变性,则蛋白质遇硫酸铜溶液后产生的沉淀,不能重新溶于水,故D错误;
故选B.
点评 本题考查了高分子化合物、糖类油脂蛋白质的性质,题目难度不大,注意葡萄糖能发生氧化反应,但葡萄糖是单糖不能发生水解.


科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
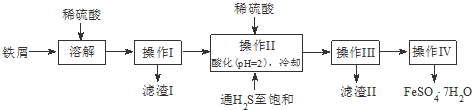
| 饱和H2S溶液 | SnS沉淀完全 | FeS开始沉淀 | FeS沉淀完全 | |
| pH值 | 3.9 | 1.6 | 3.0 | 5.5 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{\;}^{12}C$ 与${\;}_{\;}^{14}C$互为同素异形体 | |
| B. | 金刚石与石墨互为同位素 | |
| C. | 二甲醚与乙醇互为同分异构体 | |
| D. | 乙烷与乙烯互为同系物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
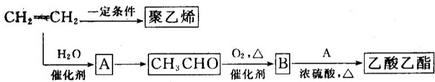
 CH3COOC2H5+H2O.
CH3COOC2H5+H2O.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
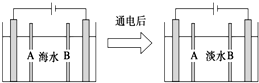
| A. | 阳离子交换膜是A,不是B | |
| B. | 通电后阳极区的电极反应式:2Cl--2e-═Cl2↑ | |
| C. | 工业上阴极使用铁丝网代替石墨碳棒,增大反应接触面 | |
| D. | 阴极区的现象是电极上产生无色气体,溶液中出现少量白色沉淀 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.2mol•L-1 | B. | 0.16mol•L-1 | C. | 0.32mol•L-1 | D. | 0.08mol•L-1 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com