
常温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.0.1 mol·L-1 NaOH溶液:K+、Ba2+、Cl-、HCO
B.0.1 mol·L-1Na2CO3溶液:K+、NH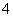 、NO
、NO 、SO
、SO
C.0.1 mol·L-1FeCl3溶液:K+、Na+、I-、SCN-
D.0.1 mol·L-1HCl的溶液:Ca2+、Na+、ClO-、NO
科目:高中化学 来源: 题型:
在P+CuSO4+H2O—→Cu3P+H3PO4+H2SO4(未配平)的反应中,7.5 mol CuSO4可氧化P的物质的量为________mol。生成1 mol Cu3P时,参加反应的P的物质的量为________mol。
查看答案和解析>>
科目:高中化学 来源: 题型:
能在水溶液中大量共存的离子组是( )
A.H+、Fe3+、SO 、I-
、I-
B.H+、NH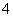 、HCO
、HCO 、NO
、NO
C.Ag+、K+、Cl-、SO
D.K+、AlO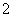 、Cl-、OH-
、Cl-、OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
水溶液中能大量共存的一组离子是( )
A.Na+、Al3+、Cl-、CO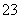
B.H+、Na+、Fe2+、MnO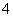
C.K+、Ca2+、Cl-、NO
D.K+、NH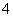 、OH-、SO
、OH-、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组离子在溶液中能够大量共存的是( )
A.NH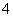 、NO
、NO 、Na+、SO
、Na+、SO
B.H+、Fe2+、Na+、NO
C.Ba2+、K+、Al3+、HCO
D.NH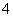 、Li+、OH-、SO
、Li+、OH-、SO
查看答案和解析>>
科目:高中化学 来源: 题型:
常见的五种盐A、B、C、D、E,它们的阳离子可能是Na+、NH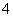 、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO
、Cu2+、Ba2+、Al3+、Ag+、Fe3+,阴离子可能是Cl-、NO 、SO
、SO 、CO
、CO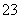 ,已知:
,已知:
①五种盐均溶于水,水溶液均为无色。
②D的焰色反应呈黄色。
③A的溶液呈中性,B、C、E的溶液呈酸性,D的溶液呈碱性。
④若在这五种盐的溶液中分别加入Ba(NO3)2溶液,只有A、C的溶液不产生沉淀。
⑤若在这五种盐的溶液中,分别加入氨水,E和C的溶液中生成沉淀,继续加氨水,C中沉淀消失。
⑥把A的溶液分别加入到B、C、E的溶液中,均能生成不溶于稀硝酸的沉淀。
请回答下列问题:
(1)五种盐中,一定没有的阳离子是____________;所含阴离子相同的两种盐的化学式是__________________。
(2)D的化学式为__________________,D溶液显碱性的原因是________________________(用离子方程式表示)。
(3)A和C的溶液反应的离子方程式是_______________________________;
E和氨水反应的离子方程式是____________________________________________。
(4)若要检验B中所含的阳离子,正确的实验方法是___________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
用如图所示装置分别进行如下实验,测定导电性变化,请按照要求选择填空。
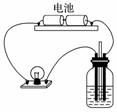
A.导电性变化不大
B.导电性明显增强
C.导电性明显减弱
D.导电性由强到弱再到强
(1)向AgNO3溶液中通入少量HCl( )
(2)向H2SO3溶液中通入Cl2( )
(3)向FeI2溶液中通入少量Cl2( )
(4)向NaOH溶液中通入少量Cl2( )
(5)向NH3·H2O中通入HCl气体( )
(6)向饱和石灰水中不断通入CO2( )
(7)向FeBr2溶液中通入少量Cl2( )
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应的离子方程式正确的是( )
A.NaAlO2溶液中滴加NaHCO3溶液:AlO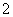 +HCO
+HCO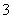 +H2O===Al(OH)3↓+CO
+H2O===Al(OH)3↓+CO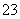
B.碘水中通入适量的SO2:I2+SO2+2H2O===2HI+SO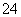 +2H+
+2H+
C.FeSO4溶液中滴加双氧水:2Fe2++2H2O2===2Fe3++O2↑+2H2O
D.Na2CO3发生水解反应:CO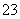 +2H2O===H2CO3+2OH-
+2H2O===H2CO3+2OH-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于微粒半径的叙述中,正确的是( )
A.金属阳离子的半径大于它的原子半径
B.金属阳离子的半径小于它的原子半径
C.非金属阴离子的半径与其原子半径相等
D.非金属阴离子的半径小于其原子半径
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com