
| A. | 5.6 g Fe 和足量的氧气完全燃烧失去电子数为 3N A | |
| B. | 1L 浓度为 0.5mol/LFeCl3 溶液加热煮沸后,会生成 0.5molFe(OH)3胶体粒子 | |
| C. | 常温常压下,23 g NO2 和 N2O4 的混合气体一定含有 N A 个氧原子 | |
| D. | 标况下,4.48L 的水中含有 H2O 分子的数目为 0.2N A |
分析 A.铁与氧气反应生成的是四氧化三铁,产物中Fe的评价化合价为+$\frac{8}{3}$;
B.氢氧化铁胶粒为氢氧化铁的聚集体;
C.NO2和N2O4的最简式均为NO2,根据最简式计算;
D.标准状况下,水的状态不是气体.
解答 解:A.5.6gFe的物质的量为:$\frac{5.6g}{56g/mol}$=0.1mol,Fe与氧气反应生成四氧化三铁,失去电子的物质的量为:0.1mol×$\frac{8}{3}$=$\frac{4}{15}$,故A错误;
B.由于氢氧化铁为氢氧化铁的聚集体,则无法计算氢氧化铁胶粒的数目,故B错误;
C.23 g NO2 和 N2O4的混合气体中含有23g最简式NO2,含有最简式NO2的物质的量为:$\frac{23g}{46g/mol}$=0.5mol,则该混合气体中含有O的物质的量为:0.5mol×2=1mol,含有氧原子数为 N A,故C正确;
D.标况下是不是气体,不能使用标况下的气体摩尔体积计算,故D错误;
故选C.
点评 本题考查阿伏加德罗常数的综合应用,题目难度中等,明确标况下气体摩尔体积的使用条件为解答关键,注意掌握好以物质的量为中心的各化学量与阿伏加德罗常数的关系,试题有利于培养学生灵活运用基础知识解决实际问题的能力.


科目:高中化学 来源: 题型:解答题
| 组 分 | SiO2 | C | Na2O | K2O | Al2O3 | Fe2O3 |
| 质量分数 | 59.20 | 38.80 | 0.25 | 0.50 | 0.64 | 0.16 |
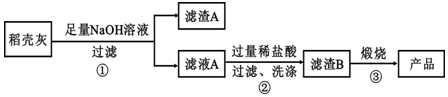
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铁与稀硫酸反应:2Fe+6H+═2Fe3++3H2↑ | |
| B. | 碳酸钙与醋酸反应:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 盐酸滴在石灰石上:CO32-+2H+═CO2↑+H2O | |
| D. | 盐酸与饱和的澄清石灰水反应:H++OH-═H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Na2SO4和 NaCl 的物质的量之比为 1:3 | |
| B. | 溶液中一定有 1molNa2SO4 和 3molNaCl | |
| C. | 所带电荷数 SO42-是 Na+的 $\frac{3}{5}$ 倍 | |
| D. | SO42-与 Cl-的物质的量之和等于 Na+的物质的量 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
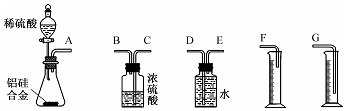
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | NaOH溶液 | B. | H2SO4溶液 | C. | MgSO4溶液 | D. | FeCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
 溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:
溴苯是一种化工原料,实验室合成溴苯的装置示意图及有关数据如下:| 苯 | 溴 | 溴苯 | |
| 密度/g•cm-3 | 0.88 | 3.10 | 1.50 |
| 沸点/℃ | 80 | 59 | 156 |
| 水中溶解度 | 微溶 | 微溶 | 微溶 |
 .d中倒置漏斗的作用是:防倒吸,某同学认为如果想验证该反应的类型,可以取反应后烧杯d中溶液,加入稀硝酸酸化,然后加入硝酸银溶液,如果产生了淡黄色沉淀即验证了该反应的类型.试分析该同学的操作是否可行:否(填“是”或“否”),简要说明其原因:进入d烧杯被NaOH溶液吸收的除了HBr外还有Br2蒸汽,加入硝酸银仅能验证d中有溴离子,但是不能说明溴离子来自于HBr还是Br2.
.d中倒置漏斗的作用是:防倒吸,某同学认为如果想验证该反应的类型,可以取反应后烧杯d中溶液,加入稀硝酸酸化,然后加入硝酸银溶液,如果产生了淡黄色沉淀即验证了该反应的类型.试分析该同学的操作是否可行:否(填“是”或“否”),简要说明其原因:进入d烧杯被NaOH溶液吸收的除了HBr外还有Br2蒸汽,加入硝酸银仅能验证d中有溴离子,但是不能说明溴离子来自于HBr还是Br2.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 苯(甲苯)KMnO4(酸化),NaOH溶液分液 | B. | 乙烷(乙烯)酸性KMnO4(溶液洗气 | ||
| C. | 乙酸乙酯(乙酸)KOH溶液分液 | D. | 苯(苯酚)浓Br2水过滤 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com