
 电化学原理广泛用于工业生产中,如有一种电化学净水法的原理是:在电解过程中将低价金属离子(如Co2+)氧化成高价态的离子(Co3+),然后以此高价态的金属离子作氧化剂把废水中的有机物氧化成CO2而净化。实验室用如图装置模拟上述过程,下列说法正确的是
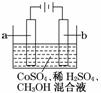
电化学原理广泛用于工业生产中,如有一种电化学净水法的原理是:在电解过程中将低价金属离子(如Co2+)氧化成高价态的离子(Co3+),然后以此高价态的金属离子作氧化剂把废水中的有机物氧化成CO2而净化。实验室用如图装置模拟上述过程,下列说法正确的是
( )
A.电极a可以是石 墨,电极b可以是铜
墨,电极b可以是铜
B.电解后阴极附近H+浓度不变
C.Co3+氧化甲醇的离子方程式为:6Co3++CH3OH+H2O===CO2↑+6Co2++6H+
D.当1 mol 甲醇被完全氧化时,阳极应该失去4 mol电子
科目:高中化学 来源: 题型:
在水溶液中能大量共存的离子组是 ( )
A.K+ 、Al3+ 、SO42-、OH- B.Ca2+ 、Na+、Cl-、NO3-
C.Na+ 、NH4+ 、NO3-、OH- D.Na+ 、H+ 、CO32-、Cl-
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关铁及其化合物的说法中正确的是
A.赤铁矿的主要成分是Fe3O4
B.铁与水蒸气在高温下的反应产物为Fe2O3和H2
C.除去FeCl2溶液中的FeCl3杂质可以向溶液中加入铁粉,然后过滤
D.Fe3+与KSCN产生血红色沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
一定量的Fe和Fe2O3混合物投入2 mol·L-1 250 mL的HNO3溶液中,反应完全后,无固体剩余,生成1.12 L NO气体(标准状况),再向反应后溶液中加入1 mol·L-1的NaOH溶液,要使铁元素全部沉淀下来,所加NaOH溶液的体积最少是
A.450 mL B.500 mL
C.400 mL  D.无法确定
D.无法确定
查看答案和解析>>
科目:高中化学 来源: 题型:
如图所示,烧杯中装有稀硫酸,A、B、C、D分别为铜、锌、碳棒、碳棒,下列说法正确的是( )
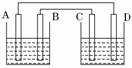
A.A、D棒上均产生气泡
B.B、C棒上均产生气泡
C.电子流动方向A→D
D.左边烧杯中溶液的pH会降低
查看答案和解析>>
科目:高中化学 来源: 题型:
下列说法正确的是( )
A.铅蓄电池放电时铅电极发生氧化反应
B.电解饱和食盐水在阳极得到氯气,阴极得到金属钠
C.给铁钉镀铜可采用CuSO4作电镀液
D.生铁浸泡在食盐水中发生析氢腐蚀
查看答案和解析>>
科目:高中化学 来源: 题型:
以下关于化学反应速率的说法正确的是( )
A、化学反应速率可用某时刻生成物的质量增加来表示
B、在同一反应中,用各种物质表示的化学反应速率的大小相等
C、化学反应速率指单位时间内反应物浓度的减少或生成物浓度的增加
D、若反应现象在短时间内出现,则反应速率快,若无明显现象,则反应速率慢
查看答案和解析>>
科目:高中化学 来源: 题型:
硫酸是一种重要的化工产品,硫酸的消耗量常被视为一个国家工业发达水平的一种标志。目前的重要生产方法是“接触法”,有关接触氧化反应2SO2+O2催化剂2SO3的说法不正确的是( )
A、该反应为可逆反应,故在一定条件下二氧化硫和氧气不可能全部转化为三氧化硫
B、达到平衡后,反应就停止了,故正、逆反应速率相等且均为零
C、一定条件下,向某密闭容器中加入2molSO2和1molO2,则从反应开始到达到平衡的过程中,正反应速率不断减小,逆反应速率不断增大,某一时刻,正、逆反应速率相等
D、在利用上述反应生产三氧化硫时,要同时考虑反应所能达到的限度和化学反应速率两方面的问题
查看答案和解析>>
科目:高中化学 来源: 题型:
不能正确表示下列反应的离子方程式的是
A.将NaHCO3液加入氯化铝溶液中 Al3+ + 3HCO3- = Al(OH)3 ↓+ 3CO2↑
B.铜与浓硝酸的反应: Cu + 4H++2NO3 - = Cu 2+ + 2NO2↑+ 2H2O
C.Ca(HCO3)2溶液与过量NaOH溶液反应:HCO3-+Ca2++OH-=CaCO3↓+H2O
D.向FeBr2溶液中通入足量氯气:2Fe2++4Br-+3Cl2=2 Fe3++2 Br2+6 Cl-
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com