
大气中的SO2是造成酸雨的主要污染物。最新研究表明,离子晶体[N(CH3)4]2 SO4(s) 能与SO2进行如下可逆反应,使其可能成为绿色的SO2吸收剂:[N(CH3)4]2 SO4(s)+ SO2(g) [N(CH3)4]2 S2O6(s)下列说法正确的是
[N(CH3)4]2 S2O6(s)下列说法正确的是
A.[N(CH3)4]+中只含共价键 B.该反应中,SO2作氧化剂
C.SO2漂白品红是利用其强氧化性 D.每吸收标准状况下的SO211.2L,生成15.4g[N(CH3)4]2 S2O6
科目:高中化学 来源: 题型:
下列有关电解质的说法中正确的是 ( )。
A.强电解质一定是离子化合物
B.强电解质、弱电解质的电离都是吸热过程
C.强电解质的饱和溶液一定是浓溶液
D.强电解质在水中一定能全部溶解
查看答案和解析>>
科目:高中化学 来源: 题型:
将一块铝硅合金恰好与NaOH溶液完全反应而溶解。
(1)写出合金溶解的离子方程式。
________________________________________________________________。
(2)向所得的溶液中加入足量的盐酸,充分反应后,溶液中大量存在的离子为
________。
查看答案和解析>>
科目:高中化学 来源: 题型:
25℃时,弱酸的电离平衡常数如表所示,下列说法正确的是
A.物质的量浓度相等的三种溶液中,pH大小关系为:
pH( NaCN)> pH(Na2 CO3 )pH(CH3 COONa)
B.amol·L-1 HCN与6 mol·L-1 NaOH溶液等体积混合所得的溶液中
c(Na+)>c(CN-),则a一定小于b
C.向冰醋酸中逐滴加水稀释的过程中,溶液导电能力先增大,后减小
D.将0.1 mol·L-1的Na2 CO3溶液逐滴加入到等浓度的HCN溶液中,无明显现象,说明未反应
查看答案和解析>>
科目:高中化学 来源: 题型:
五种短周期元素的某些性质如表所示(其中只有W、Y、Z为同周期元素)。下列说法正确的是
| 元素代号优高考网] | X | W | Y | Z | Q |
| 原子半径(×10-12 m) | 37 | 64 | 66 | 70 | 154 |
| 主要化合价 | +1 | -1 | -2 | +5、-3 | +1 |
A.由Q与Y形成的化合物中只存在离子键 B、Z与X之间形成的化合物具有还原性
C.由X、Y、Z三种元素形成的化合物,一定是共价分子 D.Y与W形成的化合物中,Y显负价
查看答案和解析>>
科目:高中化学 来源: 题型:
几种短周期元素的原子半径及主要化合价如下表:
| 元素代号 | X | Y | Z | M | R | Q | |
| 原子半径(×10-10 m) | 1.86 | 0.99 | 1.43 | 1.60 | 0.75 | 0.74 | |
| 主要 化合价 | 最高正价 | +1 | +7 | +3 | +2 | +5 | — |
| 最低负价 | — | -1 | — | — | -3 | -2 |
下列说法正确的是 ( )。
A.X、Z、R的最高价氧化物的水化物之间可两两相互反应
B.元素X和Q形成的化合物中不可能含有共价键
C.X、Z、M的单质分别与水反应,Z最剧烈
D.Y的氢化物的水溶液可用于蚀刻玻璃
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关叙述正确的是()
A. 氢键是一种特殊化学键,它广泛地存在于自然界中
B. 在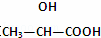 分子中含有1个手性C原子
分子中含有1个手性C原子
C. 碘单质在水溶液中溶解度很小是因为I2和H2O都是非极性分子
D. 含氧酸可用通式XOm(OH)n来表示,若n值越大,则含氧酸的酸性越大
查看答案和解析>>
科目:高中化学 来源: 题型:
下面是几种有机物的结构简式:
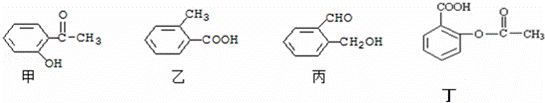
其中,(1)互为同分异构体的有 (从甲、乙、丙、丁中选出).
(2)能与NaHCO3溶液反应的有: ;能够发生水解反应的有: .
(3)写出丙中含有的含氧官能团的名称 .
(4)请写出鉴别甲的方法(指明所选试剂及主要现象): .
(5)写出丙物质发生银镜反应的化学方程式: .
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com