
将X气体通入BaCl2溶液,未见沉淀生成,然后通入Y气体,有沉淀生成,X、Y不可能是
| 选项 | X | Y |
| A | SO2 | H2S |
| B | Cl2 | CO2 |
| C | NH3 | CO2 |
| D | SO2 | Cl2 |
科目:高中化学 来源: 题型:
已知A是一种装饰品的主要成 分,根据下图转化关系,回答下列问题。
分,根据下图转化关系,回答下列问题。
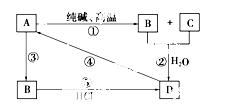
(1)A用途______________(任写一种),B是________,D是________。
(2)写出化学方程式
①________________________________________________________________________。
④________________________________________________________________________。
(3)写出离子方程式
②________________________________________________________________________。
③________________________________________________________________________。
⑤________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
(有机化学基础)蜂胶是一种天然抗癌药物,一个五六万只的蜂群一年只能产100多克蜂胶,所以蜂胶又被誉为“紫色黄金”。蜂胶的主要活性成分为咖啡酸苯乙酯,其分子结构如右图所示(短线表示化学键,如单键、双键等),在一定条件下能发生如下转化。
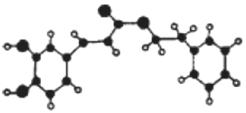
请回答下列问题:
(1)咖啡酸苯乙酯的分子式为 .C的结构简式为
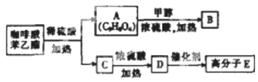
(2)①A中含氧官能团的名称为 、 。
②A可以发生的反应是 (填字毋)。
A、 加成反应B、酯化反应C、消去反应D、氧化反应
(3)高分子E的结构简式是 。
(4)C→D发生反应的反应类型是 。
(5)B的同分异构体有很多种,其中同时符合下列条件的同分异构体的结构简式为 。
a、苯环上只有两个取代基b.能发生银镜反应 c、能与氢氧化钠溶液反应
d、不能与氯化铁溶液发生显色反应 e、核磁共振氢谱图中有三组峰
查看答案和解析>>
科目:高中化学 来源: 题型:
氯气溶于水达到平衡后,若其他条件不变,只改变某一条件,下列叙述正确的是
A.再通入少量氯气,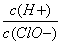 减小
减小
B.通入少量SO2,溶液漂白性增强
C.加入少量固体NaOH,一定有c(Na+)=c(Cl-)+c(ClO-)
D.加入少量水,水的电离平衡向正反应方向移动
查看答案和解析>>
科目:高中化学 来源: 题型:
常温下,A是可用来对自来水进行消毒的黄绿色单质气体,A、B、C、D、E都含X元素,其转化关系如图所示。
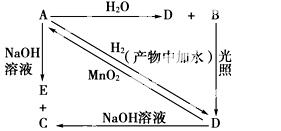
(1)请分别写出A、B、D的化学式(如为溶液请填溶质的化学式):
A________、B________、D________;
(2)写出下列反应的化学方程式或离子方程式(请注明条件):
A+H2O(离子方程式):_________________________________________________;
A+NaOH(离子方程式):________________________________________________;
D→A(化学方程式):__________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室常用MnO2与浓盐酸反应制备Cl2(发生装置如图所示)。
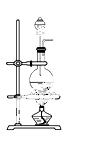 (1)制备实验开始时,先检查装置气密性,接下来的操作依次是_______(填序号)。
(1)制备实验开始时,先检查装置气密性,接下来的操作依次是_______(填序号)。
A.往烧瓶中加入MnO2粉末
B.加热
C.往烧瓶中加入浓盐酸
(2)制备反应会因盐酸浓度下降而停止。为测定反应残余液中盐酸的浓度,
探究小组同学提出下列实验方案:
甲方案:与足量AgNO3溶液反应,称量生成的AgCl质量。
乙方案:采用酸碱中和滴定法测定。
丙方案:与已知量CaCO3(过量)反应,称量剩余的CaCO3质量。
丁方案:与足量Zn反应,测量生成的H2体积。
继而进行下列判断和实验:
①判定甲方案不可行,理由是____________________________________________。
②进行乙方案实验:准确量取残余清液稀释一定倍数 后作为试样。
后作为试样。
 a.量取试样20.00 mL,用0.100 0 mol·L-1 NaOH标准溶液滴定,消耗22.00 mL,该次滴定测得试样中盐酸浓度为__________mol·
a.量取试样20.00 mL,用0.100 0 mol·L-1 NaOH标准溶液滴定,消耗22.00 mL,该次滴定测得试样中盐酸浓度为__________mol· L-1;
L-1;
b.平行滴定后获得实验结果。
③判断丙方案的实验结果________(填“偏大”、“偏小”或“准确”)。
[已知:Ksp(CaCO3)=2.8×10-9、Ksp(MnCO3)=2.3×10-11]
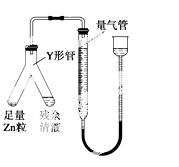
④进行丁方案实验:装置如右图所示(夹持器具已略去)。
(ⅰ) 使Y形管中的残余清液与锌粒反应的正确操作是将________ 转移到________中。
(ⅱ)反应完毕,每间隔1分钟读取气体体积,气体体积逐次减小,直至不变。气体体积逐次减小的原因是_____________
(排除仪器和实验操作的影响因素)。
查看答案和解析>>
科目:高中化学 来源: 题型:
9.3-氯戊烷是一种有机合成中间体,下列有关3-氯戊烷的叙述正确的是
A.3-氯戊烷的分子式为C6H9Cl3 B.3-氯戊烷属于烷烃
C.3-氯戊烷的一溴代物共有3种 D.3-氯戊烷的同分异构体共有6种
查看答案和解析>>
科目:高中化学 来源: 题型:
海水是巨大的化学资源库,下列有关海水综合利用说法正确的是( )。
A.海水的淡化,只需经过化学变化就可以得到
B.海水蒸发制海盐的过程中只发生了化学变化
C.从海水中可以得到NaCl,电解熔融NaCl可制备金属Na
D.利用海水、铝、空气的航标灯的原理是将电能转化为化学能
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,发出苍白色火焰,产物溶于水得到一种强酸。回答下列问题:
(1)写出一种工业制备单质F的化学方程式:____________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为___________, 请用离子方程式解释该溶液呈碱性的原因____________________________________________;
(3)实验室用F从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
|
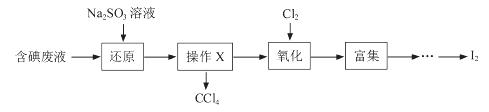
①向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为__________ ;
②操作X的名称为___________________。
③已知:5SO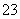 +2IO
+2IO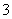 +2H+===I2+5SO
+2H+===I2+5SO +H2O,某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO
+H2O,某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO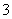 中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO
中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO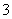 的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验没有碘单质存在;___________________________________;
的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验没有碘单质存在;___________________________________;
另从水层取少量溶液,加入1~2 mL淀粉溶液,加盐酸酸化,滴加Na2SO3溶液,若溶液变蓝,说明废水中含有IO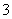 ;若溶液不变蓝,说明废水中不含有IO
;若溶液不变蓝,说明废水中不含有IO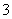 。
。
(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液。)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com