
【题目】已知:A、B、C、D四种元素,原子序数依次增大。A是短周期中原子半径最大的元素,B元素3p能级半充满;C是所在周期电负性最大的元素;D是第四周期未成对电子最多的元素。试回答下列有关的问题:
(1)写出D元素价电子的电子排布式:______________。
(2)D可形成化合物[D(H2O)6](NO3)3 。
①[D(H2O)6](NO3)3中阴离子的立体构型是_____________。NO3-中心原子的轨道杂化类型为__________。
②在[D(H2O)6] 3+中D3+与H2O之间形成的化学键称为______,1 mol [D(H2O)6] 3+ 中含有的σ键有________mol。
(3)已知B、C两种元素形成的化合物通常有两种。这两种化合物中________(填化学式)为非极性分子。另一种物质的电子式为_____________。
(4)由A、C两元素形成的化合物组成的晶体中,阴、阳离子都具有球型对称结构,它们都可以看做刚性圆球,并彼此“相切”。如下图所示为A、C形成化合物的晶胞结构图以及晶胞的剖面图:

晶胞中距离一个A+最近的C-有________个,这些C-围成的图形是______________,若晶体密度为ρ g·cm-3,阿伏加德罗常数的值用NA表示,则A+的离子半径为________cm(用含NA与ρ的式子表达)。
【答案】 3d54s1 平面三角形 sp2杂化 配位键 18 PCl5 ![]() 6 正八面体
6 正八面体 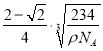
【解析】A、B、C、D四种元素,原子序数依次增大。A是短周期中原子半径最大的元素,A为Na元素;B元素3p能级半充满,B为P元素。D是第四周期未成对电子最多的元素,D为Cr元素;C是所在周期电负性最大的元素,C为第ⅦA族元素,C为Cl元素。
(1)D为Cr元素,D元素价电子的电子排布式为3d54s1,故答案为:3d54s1;
(2)①[D(H2O)6](NO3)3中NO3- NO3-中价层电子对个数=3+![]() (5+1-3×2)=3,且不含孤电子对,所以该分子为平面三角形,中心原子采用sp2杂化,故答案为:平面三角形;sp2杂化;
(5+1-3×2)=3,且不含孤电子对,所以该分子为平面三角形,中心原子采用sp2杂化,故答案为:平面三角形;sp2杂化;
②在[Cr (H2O)6] 3+配合离子中Cr3+与H2O之间形成的化学键为配位键;水分子中含有σ键2×6=12,配位键也是σ键,1 mol [D(H2O)6] 3+ 中含有的σ键有12+6=18mol,故答案为:18;
(3)已知B、C两种元素形成的化合物为PCl3和PCl5,PCl3为三角锥形结构,属于极性分子,PCl5为三角双锥结构,属于非极性分子,其中PCl3的电子式为![]() ,故答案为:PCl5;
,故答案为:PCl5; ![]() ;
;
(4)由Na、Cl两元素形成的化合物为NaCl,以中间的黑色球为Na+离子研究,与之最近的氯离子有6个,这些氯离子围成的图形是正八面体;晶胞中Na+离子数目=1+12×![]() =4,Cl-离子数目=8×
=4,Cl-离子数目=8×![]() +6×
+6×![]() =4,故晶胞质量=
=4,故晶胞质量=![]() g,晶胞体积=[
g,晶胞体积=[![]() g÷ρ]cm3=
g÷ρ]cm3=![]() cm3,令Na+离子半径为r,则棱长为
cm3,令Na+离子半径为r,则棱长为![]() ×4r=2
×4r=2![]() r,故(2
r,故(2![]() r)3=
r)3=![]() cm3,解得r=
cm3,解得r=![]() ×
×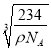 cm,故答案为:6;
cm,故答案为:6; ![]() ×
×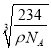 。
。


 学业测评一课一测系列答案
学业测评一课一测系列答案 小学课时作业全通练案系列答案
小学课时作业全通练案系列答案科目:高中化学 来源: 题型:
【题目】化学反应原理在工业生产中具有十分重要的意义。
工业生产可以用NH3(g)与CO2(g)经两步反应生成尿素,两步反应的能量变化示意图如下:

(1)则NH3 (g)与CO2(g)反应生成尿素的热化学方程式为______________________________。
(2)已知反应Fe(s)+CO2(g) ![]() FeO(s)+CO(g) ΔH =a kJ·mol-1。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
FeO(s)+CO(g) ΔH =a kJ·mol-1。测得在不同温度下,该反应的平衡常数K随温度的变化如下:
温度(℃) | 500 | 700 | 900 |
K | 1. 00 | 1.47 | 2.40 |
①该反应的化学平衡常数K的表达式为____________,a________0(填“>”、“<”或“=”)。在500 ℃ 2 L密闭容器中进行反应,Fe和CO2的起始量均为4 mol,则5 min后达到平衡时CO2的转化率为________,生成CO的平均速率v (CO)为__________________。
②700 ℃反应达到平衡后,要使反应速率增大且平衡向右移动,可采取的措施有____________________。
(3) 利用CO与H2可直接合成甲醇,下图是由“甲醇-空气”形成的绿色燃料电池的工作原理示意图,写出以石墨为电极的电池工作时负极的电极反应式_______________________,利用该电池电解1L 0.5mol/L的CuSO4溶液,当消耗560mLO2 (标准状况下),电解后溶液的pH=_______(溶液电解前后体积的变化忽略不计)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素化合价与原子序数的关系图,请根据图中给出的信息,指出下列有关说法中正确的是

(纵坐标为化合价的变化,横坐标为原子序数的变化)
A. 原子半径:W>Z>Y
B. 气态氢化物的稳定性:H2X<H2W
C. Y2X和水反应能生成离子化合物
D. Y和Z两者氧化物对应的水化物不能相互反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,CH4与H2O(g)发生反应:CH4(g)+H2O(g) ![]() CO(g)+3H2(g),设起始
CO(g)+3H2(g),设起始![]() =Z,在恒压下,平衡时
=Z,在恒压下,平衡时![]() (CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是( )
(CH4)的体积分数与Z和T(温度)的关系如图所示。下列说法正确的是( )

A.该反应的焓变ΔH>0
B.图中Z的大小为a>3>b
C.图中X点对应的平衡混合物中![]() =3
=3
D.温度不变时,图中X点对应的平衡在加压后![]() (CH4)减小
(CH4)减小
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在体积均为1.0 L的两恒容密闭容器中加入足量的相同的碳粉,再分别加入0.1 mol CO2和0.2 mol CO2,在不同温度下反应 CO2(g)+C(s) ![]() 2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如下图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )
2CO(g)达到平衡,平衡时CO2的物质的量浓度c(CO2)随温度的变化如下图所示(图中Ⅰ、Ⅱ、Ⅲ点均处于曲线上)。下列说法正确的是( )

A.反应 CO2(g)+C(s) ![]() 2CO(g)的 ΔS>0、 ΔH<0
2CO(g)的 ΔS>0、 ΔH<0
B.体系的总压强p总:p总(状态Ⅱ) <2p总(状态Ⅰ)
C.体系中 c(CO):c(CO,状态Ⅱ)<2c(CO,状态Ⅲ)
D.逆反应速率v逆: v逆(状态Ⅰ)>v逆(状态Ⅲ)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,容积为2 L的恒容密闭容器中,通入2 mol N2、3 mol H2进行反应N2(g)+3H2(g) ![]() 2NH3(g),20 min后,N2的物质的量为1.9 mol,1 h后测得容器内气体的压强不再改变,且为反应开始时压强的0.8倍,则下列叙述正确的是:
2NH3(g),20 min后,N2的物质的量为1.9 mol,1 h后测得容器内气体的压强不再改变,且为反应开始时压强的0.8倍,则下列叙述正确的是:
A.当容器内压强不改变时,说明反应已达到平衡状态
B.增加H2的浓度或降低温度,平衡将向正反应方向移动,且反应速率均加快
C.前20 min用NH3表示的反应速率为0.01 mol·L-1·min-1
D.1 h后反应进行完全,容器中的N2浓度为0.55 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.96 g铜片加入500 mL0.2 mol/L稀硝酸中,充分反应,现欲使溶液中的Cu2+全部转化为Cu(OH)2沉淀,应加入0.2 mol/L NaOH溶液体积为( )
A. 300 mL B. 400 mL C. 450 mL D. 500 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,用浓度为0.1000mol/L的盐酸分别逐滴加入到20.00mL 0.1000mol/L的两种一元碱MOH、ROH溶液中,PH随盐酸溶液体积的变化如图所示。下列说法正确的是

A. PH=10时,c(M+)>c(MOH)>c(Cl-)>c(OH-)>c(H+)
B. 将上述MOH、ROH溶液等体积混合后,用盐酸滴定至MOH恰好反应时:c(R+)>c(M+)>c(H+)>c(OH-)
C. 10mL<V(HCl)<20mL时,c(M+)+c(NOH)<c(Cl-)
D. V(HCl)>20mL时,不可能存在:c(Cl-)>c(M+)=c(H+)>c(OH-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】控制适合的条件,将反应2Fe3++2I-![]() 2Fe2++I2设计成如图所示的原电池。下列判断不正确的是:
2Fe2++I2设计成如图所示的原电池。下列判断不正确的是:

A.反应开始时,乙中石墨电极上发生氧化反应
B.反应开始时,甲中石墨电极上Fe3+被还原
C.电流计读数为零时,反应达到化学平衡状态
D.电流计读数为零后,在甲中溶入FeCl2固体,乙中石墨电极为负极
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com