
| A�� | f��g��k��m | B�� | c��j��k��m | C�� | c��h��i��k | D�� | f��g��h��j�� |
���� �ζ�����ʱ���ζ��ܱ���ʹ�ô�װҺ��ϴ����ƿ������ϴ���ζ�ʱ�۾�Ӧ��ע����ƿ�л��Һ��ɫ�仯���ζ��յ�����Ϊ��Һ����ɫ��ɷۺ�ɫ�Ұ���Ӳ���ɫ���ζ��ܶ���Ӧ�ö���0.01mL��
��� �⣺c��������NaOH��Һ����ʽ�ζ���������ˮϴ�꣬����ʹ�ô�װҺ��ϴ��������ȡ����������Һ����c����
j����ע�ӵζ�����Һ��仯���ò������ζ�ʱ�۾�Ӧ��ע����ƿ����Һ��ɫ�仯���Ա㼰ʱ�жϴﵽ�յ㣬��j����
k����С�ĵε���Һ����ɫ��ɷۺ�ɫ�Ұ���Ӳ���ɫʱ������ֹͣ�ζ���������ǰ�����ζ���Ӱ��ζ��������k����
m���ζ���ȷ��Ϊ0.01mL���ζ��ܵ����ζ����ó�NaOH��Һ�����Ӧ��Ϊ22.00mL����m����
��ѡB��
���� ���⿼�黯ѧʵ�鷽�������ۣ���Ҫ����������ԭ�ζ��IJ��������������������ѶȲ���ע��ʵ��Ļ���������������淶�Ժ�ע�����ע�⣺�ζ�ʱ�۾�ע����ƿ��Һ����ɫ�仯�����ǵζ�����Һ��仯��Ϊ�״��㣮



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ȼ����Ϊ890.3kJ•mol-1�������ȼ�յ��Ȼ�ѧ����ʽ�ɱ�ʾΪ��CH4��g��+2O2��g���TCO2��g��+2H2O��g����H=-890.3kJ•mol-1 | |
| B�� | 500�桢30MPa�£���0.5molN2��g����1.5molH2��g�������ܱ������г�ַ�Ӧ����NH3��g������19.3kJ�����Ȼ�ѧ����ʽΪ��N2��g��+3H2��g��?2NH3��g����H=-38.6kJ•mol-1 | |
| C�� | HCl��NaOH��Ӧ���к��ȡ�H=-57.3kJ•mol-1����H2SO4��Ca��OH��2��Ӧ���к��ȡ�H=2����-57.3��kJ•mol-1 | |
| D�� | ��101kPaʱ��2gH2��ȫȼ������Һ̬ˮ���ų�285.8kJ����������ȼ�յ��Ȼ�ѧ����ʽ��ʾΪ��2H2��g��+O2��g���T2H20��l����H=-571.6kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.3g��������һ������������Na2O��Na2O2�Ļ����ʱ����ʧȥ�ĵ�����ĿΪ0.1NA | |
| B�� | 22.4L�����������ķ�����ĿΪNA | |
| C�� | 1mol/L Na2CO3��Һ�к���Na+������Ŀ��NA | |
| D�� | 17g������������ԭ����ĿΪ4NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ���·������������ۻ�Ϊͬ���칹�� | |
| B�� | ��ըʳ��Ļ����ͺ�ţ�Ͷ��ǿ����������� | |
| C�� | �ϳ�������ά�������л��߷��Ӳ��� | |
| D�� | ĥ�����Ĵ��������ʣ�������к��ʱ���˰����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
| Ҫ�ᴿ������ �����ʣ� | ���� ����ϩ�� | �������� �����ᣩ | �Ҵ� ��ˮ�� | �屽 ���壩 |
| ѡ���Լ� | ||||
| ���뷽�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BF3 | B�� | NH4+ | ||
| C�� | CCl4 | D�� | ������еĹ�ԭ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ���ѡ��
| A�� | 13g��Ȳ��C2H2����ԭ����Ϊ2NA | |
| B�� | 4��ʱ9mLˮ��11.2L����������ͬ�ķ����� | |
| C�� | ͬ��ͬѹ�£�NA��NO2��NA��N2�������� | |
| D�� | ��״���£�11.2 L����������ԭ����ĿΪNA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
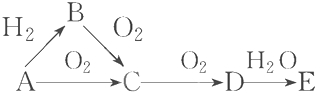
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com