
【题目】一块表面被氧化的铝分成两等分,若向其中一份中滴加1molL-1的NaOH溶液,向另一份中滴加x molL-1的稀盐酸,产生氢气的物质的量与所加NaOH溶液、稀盐酸的体积关系如图所示.下列说法不正确的是( )
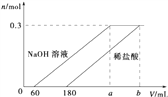
A. a=260
B. x=1mol/L
C. 该铝块的总质量为8.46g
D. 该铝块中氧化铝与铝单质的物质的量之比为3:20
【答案】C
【解析】分析可知,铝与盐酸、铝与氢氧化钠都是2 mol铝产生3 mol氢气;A、产生0.3mol氢气,消耗0.2mol氢氧化钠,NaOH的浓度是1mol/L,V(NaOH)=200mL,加上与氧化铝反应的60mL,求出a=260,A项正确;B、预想求出稀盐酸的浓度x,需利用2mol NaOH~1molAl2O3的关系求出n(Al2O3)=0.03mol,再根据1molAl2O3~6HCl,求出n(HCl)=0.18mol,x=1mol/L,B项正确;C、与NaOH反应的Al2O3是0.03mol,产生0.3mol氢气,需要0.2mol铝,一份铝块的质量=m(Al2O3)+m(Al)=8.46g,总质量为8.46![]() 2=16.92g,C项错误; D、根据与氢氧化钠反应的氧化铝0.03mol,与氢氧化钠反应的铝0.2mol,所以氧化铝与铝单质的物质的量之比为3:20,D项正确;答案选C。
2=16.92g,C项错误; D、根据与氢氧化钠反应的氧化铝0.03mol,与氢氧化钠反应的铝0.2mol,所以氧化铝与铝单质的物质的量之比为3:20,D项正确;答案选C。


 教学练新同步练习系列答案
教学练新同步练习系列答案 课前课后同步练习系列答案
课前课后同步练习系列答案 课堂小作业系列答案
课堂小作业系列答案 黄冈小状元口算速算练习册系列答案
黄冈小状元口算速算练习册系列答案 成功训练计划系列答案
成功训练计划系列答案 倍速训练法直通中考考点系列答案
倍速训练法直通中考考点系列答案科目:高中化学 来源: 题型:
【题目】某原电池装置如图所示。下列有关叙述中,正确的是 ( )

A. Fe作正极,发生氧化反应
B. 负极反应:2H++2e-===H2↑
C. 工作一段时间后,两烧杯中溶液pH均不变
D. 工作一段时间后,NaCl溶液中c(Cl-)增大
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某兴趣小组的同学用如图所示装置研究有关电化学的问题.当闭合装置的电键时,观察到电流表的指针发生了偏转.请回答下列问题:

(1)甲装置的名称是 ______ ;Pt为 ______ 极(A.正B.负C.阳D.阴).
(2)写出电极反应式:Cu极 ______ ,C极 ______ .
(3)若乙中电极不变,将其溶液换成饱和NaCl溶液,乙中溶液的总反应的离子方程式为 ______ ;若要使溶液恢复到原饱和溶液的浓度,需要加入的物质是 ______ (填名称);
(4)若乙中电极不变,将其溶液换成饱和CuSO4溶液,当甲中产生0.1mol气体时,线路中转移的电子数是 ______ ;乙中溶液H+的浓度是 ______ (假设溶液体积是200mL,且电解过程中溶液体积不变).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向100mL 1mol/LCa(HCO3)2溶液中投入Na,当沉淀最大量时,至少需要Na的质量是( )g
A. 2.3 B. 4.6 C. 1.15 D. 4
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】甲,乙两份等质量的NaHCO3固体,将甲充分加热后,再加入足量盐酸,乙不加热也加入足量盐酸,反应完全后,甲,乙两份中实际参加反应的盐酸的质量比为
A. 1∶1.5 B. 1∶1 C. 1∶2 D. 2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将铁棒和锌棒用导线连接插入硫酸铜溶液中,当电池中有0.4 mol电子通过时,负极的质量变化是
A.增加6.5g B.减少5.6g C.增加11.2g D.减少13g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在容积为1.00L的容器中,通入一定量的N2O4,发生反应N2O4(g)2NO2(g),随温度升高,混合气体的颜色变深。回答下列问题:
(1)反应的△H_____0(填“大于”“小于”);100℃时,体系中各物质浓度随时间变化如下图所示。在0-60s时段,反应速率v(N2O4)为_____molL-1s-1反应的平衡常数K1为_______。

(2)100℃时达到平衡后,改变反应温度为T,c(N2O4)以0.0020 molL-1s-1的平均速率降低,经10s又达到平衡。
①T_____100℃(填“大于”“小于”),判断理由是___________________________。
②列式计算温度T时反应的平衡常数K2_______________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com