
¹ŲÓŚŌ×Ó½į¹¹”¢ŌŖĖŲŠŌÖŹµÄĖµ·ØÕżČ·µÄŹĒ
A£®ĖęŌ×ÓŠņŹżµÄµŻŌö£¬ŌŖĖŲŌ×ÓµÄŗĖĶāµē×ÓŹżÖš½„Ōö¶ą£¬Ō×Ó°ė¾¶Öš½„¼õŠ”
B£®ČōĮ½ÖÖ²»Ķ¬µÄŗĖĖŲ¾ßÓŠĻąĶ¬µÄÖŠ×ÓŹż£¬Ōņ¶žÕßŅ»¶Ø²»ŹōÓŚĶ¬ÖÖŌŖĖŲ
C£®ČōĮ½ÖÖŌŖĖŲŌ×ÓµÄ×īĶā²ćµē×ÓŹżĻąĶ¬£¬ŌņŌŖĖŲ×īøßÕż¼ŪŅ»¶ØĻąĶ¬
D£®µē×Ó²ć½į¹¹ĻąĶ¬µÄĪ¢Į££¬Ęä»ÆѧŠŌÖŹŅ»¶ØĻąĖĘ
B
”¾½āĪö”æ
ŹŌĢā·ÖĪö£ŗA”¢ŌŖĖŲµÄŌ×Ó°ė¾¶Óėµē×Ó²ćŹż¼°ŗĖµēŗÉŹżÓŠ¹Ų£¬µē×Ó²ćŹżŌ½¶ą£¬µē×ÓÖ®¼äµÄøŗµēÅųā½«Ź¹Ō×ӵİė¾¶Ōö“ó£¬ŗĖµēŗÉŹżŌ½“ó£¬ŗĖ¶Ōµē×ÓµÄŅżĮ¦Ņ²Ō½“󣬽«Ź¹Ō×ӵİė¾¶ĖõŠ”£¬¹ŹA“ķĪó£»B”¢ČōĮ½ÖÖ²»Ķ¬µÄŗĖĖŲ¾ßÓŠĻąĶ¬µÄÖŠ×ÓŹż£¬ŌņŅ»¶ØƻӊĻąĶ¬µÄÖŹ×ÓŹż£¬·ńŌņĪŖĶ¬Ņ»ÖÖŌŖĖŲ£¬ÖŹ×ÓŹż²»Ķ¬£¬ŌņĪŖ²»Ķ¬µÄŌŖĖŲ£¬¹ŹBÕżČ·£»C”¢ČōĮ½ÖÖŌŖĖŲŌ×ÓµÄ×īĶā²ćµē×ÓŹżĻąĶ¬£¬ŌņŌŖĖŲ×īøßÕż¼Ū²»Ņ»¶ØĻąĶ¬£¬ČēKŗĶCuµÄ×īĶā²ćµē×ÓŹż¶¼ŹĒ1£¬¶ųKµÄ×īøßÕż¼ŪŹĒ+1¼Ū£¬ĶµÄ×īøßÕż¼ŪŹĒ+2¼Ū£¬¹ŹC“ķĪó£»D”¢µē×Ó²ć½į¹¹ĻąĶ¬µÄĪ¢Į££¬ČēK+ŗĶCl-µÄµē×Ó²ć½į¹¹ĻąĶ¬£¬¶ųĘä»ÆѧŠŌÖŹ²»Ķ¬£¬¹ŹD“ķĪó”£
æ¼µć£ŗ±¾Ģāæ¼²éŌ×Ó½į¹¹ÓėŌŖĖŲµÄŠŌÖŹ”£



| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģɽ¶«Ź”øßČżÉĻѧʌµŚ¶ž“Ī¼ģ²ā»ÆѧŹŌŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
·“Ó¦¢Ł”¢¢Ś·Ö±šŹĒ“Óŗ£Ōå»ŅŗĶijÖÖæóŹÆÖŠĢįČ”µāµÄÖ÷ŅŖ·“Ó¦£ŗ
¢Ł2NaI+MnO2+3H2SO4==2NaHSO4+MnsO4+2H2O+I2
¢Ś2NaIO3+5NaHSO3==2Na2SO4+3NaHSO4+H2O+I2
ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ
A£®Į½øö·“Ó¦ÖŠNaHSO4¾łĪŖŃõ»Æ²śĪļ
B£®µāŌŖĖŲŌŚ·“Ó¦¢ŁÖŠ±»»¹Ō£¬ŌŚ·“Ó¦¢ŚÖŠ±»Ńõ»Æ
C£®Ńõ»ÆŠŌ£ŗMnO2>SO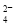 >IO
>IO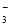 >I2
>I2
D£®·“Ó¦¢Ł”¢¢ŚÖŠÉś³ÉµČĮæµÄI2Ź±×ŖŅʵē×ÓŹż±ČĪŖ1£ŗ5
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģɽ¶«Ź”ĪĵĒŹŠøßČżÉĻѧʌ11ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£ØB¾ķ£©£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠÓŠ¹ŲĶ¼ĻńµÄŠšŹö“ķĪóµÄŹĒ
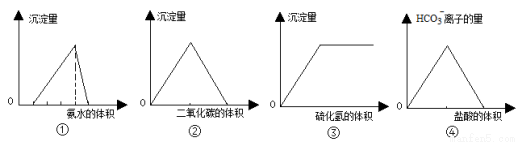
A£®¢ŁĶ¼æɱķŹ¾ĻņĖį»ÆµÄAlCl3ČÜŅŗÖŠÖšµĪ¼ÓČėĻ”°±Ė®£¬³ĮµķĮæÓė°±Ė®Ģå»żµÄ¹ŲĻµ
B£®¢ŚĶ¼ÖŠæɱķŹ¾Ļņ³ĪĒåŹÆ»ŅĖ®ÖŠĶØČė¶žŃõ»ÆĢ¼ĘųĢ壬³ĮµķĮæÓė¶žŃõ»ÆĢ¼Ģå»żµÄ¹ŲĻµ
C£®¢ŪĶ¼ÖŠæɱķŹ¾ĻņŃĒĮņĖįČÜŅŗÖŠĶØČėĮņ»ÆĒā£¬³ĮµķĮæÓėĮņ»ÆĒāĘųĢåµÄ¹ŲĻµ
D£®¢ÜĶ¼ÖŠæɱķŹ¾ĻņĢ¼ĖįÄĘČÜŅŗÖŠÖšµĪ¼ÓČėĻ”ŃĪĖį£¬HCO3£Ąė×ÓµÄĮæÓėŃĪĖįĢå»żµÄ¹ŲĻµ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģɽ¶«Ź”µĀÖŻŹŠøßČżĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
(16·Ö)ŅŃÖŖX”¢Y”¢Z”¢M”¢G”¢QŹĒĮłÖÖ¶ĢÖÜĘŚŌŖĖŲ£¬Ō×ÓŠņŹżŅĄ“ĪŌö“ó”£X”¢Z”¢QµÄµ„ÖŹŌŚ³£ĪĀĻĀ³ŹĘųĢ¬£»YµÄŌ×Ó×īĶā²ćµē×ÓŹżŹĒĘäµē×Ó²ćŹżµÄ2±¶£»XÓėMĶ¬Ö÷×壻ZµÄĘųĢ¬Ēā»ÆĪļÄÜÓėĘä×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļ·“Ó¦£¬GŹĒµŲæĒÖŠŗ¬Įæ×īøߵĽšŹōŌŖĖŲ”£
Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Y”¢Z”¢M”¢GĖÄÖÖŌŖĖŲŌ×Ó°ė¾¶Óɓ󵽊”µÄĖ³ŠņŹĒ(Š“ŌŖĖŲ·ūŗÅ) ”£
£Ø2£©ZŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖ ”£
£Ø3£©ÉĻŹöŌŖĖŲµÄ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦µÄĖ®»ÆĪļĖįŠŌ×īĒæµÄŹĒ(Š“»ÆѧŹ½) ”£
£Ø4£©³£ĪĀĻĀ£¬²»ÄÜÓėGµÄµ„ÖŹ·¢Éś·“Ó¦µÄŹĒ(ĢīŠņŗÅ) ”£
a£®CuSO4ČÜŅŗ b£®Fe2O3 c£®ÅØĮņĖį d£®NaOHČÜŅŗ e£®Na2CO3¹ĢĢå
£Ø5£©ŅŃÖŖ»ÆŗĻĪļCŗ¬ÓŠĻĀŹöŌŖĖŲÖŠµÄijŅ»ÖÖŌŖĖŲ
¢ŁČōDŹĒŅ»ÖÖĒæĖį£¬ŌņCÓėĖ®·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ ”£
ÓŠČĖČĻĪŖ”°ÅØH2SO4æÉŅŌøÉŌļĘųĢåC”±£¬Ä³Ķ¬Ń§ĪŖĮĖŃéÖ¤øĆ¹ŪµćŹĒ·ńÕżČ·£¬ÓĆČēĶ¼×°ÖĆ½ųŠŠŹµŃ飮·ÖŅŗĀ©¶·ÖŠÓ¦¼ÓČė £¬“ņæŖ·ÖŅŗĀ©¶·½ųŠŠŹµŃ飬¹ż³ĢÖŠ£¬ÅØH2SO4ÖŠĪ“·¢ĻÖÓŠĘųĢåŅŻ³ö£¬ĒŅ±äĪŖŗģ×ŲÉ«£¬ŌņÄćµĆ³öµÄ½āŹĶŗĶ½įĀŪŹĒ ”£
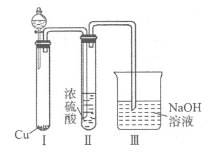
¢ŚČōDŹĒŅ»ÖÖ³£¼ūµÄĒæ¼ī£¬ŌņCÓėĖ®·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģɽ¶«Ź”µĀÖŻŹŠøßČżĘŚÖŠæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
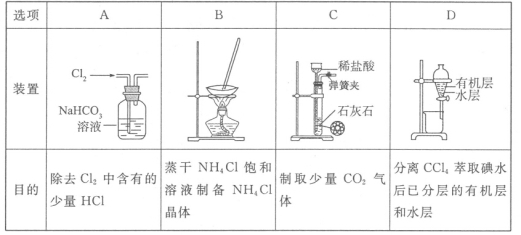
ÓĆĻĀĮŠ×°ÖĆ½ųŠŠĻąÓ¦ŹµŃ飬ÄÜ“ļµ½ŹµŃéÄæµÄµÄŹĒ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģɽ¶«Ź”µĀÖŻŹŠøßČż10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
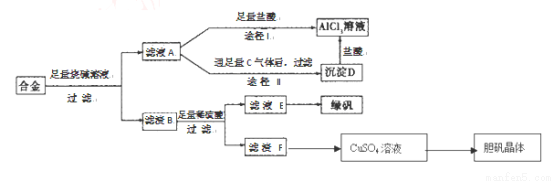
£Ø9·Ö£©Ä³»ÆѧŠĖȤŠ”×éÓĆŗ¬ÓŠĀĮ”¢Ģś”¢ĶµÄŗĻ½šÖĘČ”“æ¾»µÄĀČ»ÆĀĮČÜŅŗ”¢ĀĢ·Æ¾§Ģå£ØFeSO4”¤7H2O£©ŗĶµØ·Æ¾§Ģ壬ŅŌĢ½Ė÷¹¤Ņµ·ĻĮĻµÄŌŁĄūÓĆ”£Ę䏵Ńé·½°øČēĻĀ£ŗŹŌ»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Ę÷²ÄŅŃÓŠ£ŗĀĖÖ½”¢Ģś¼ÜĢØ”¢ĢśČ¦ŗĶÉÕ±£¬»¹ŅŖ²¹³äµÄ²£Į§ŅĒĘ÷ŹĒ£ØĢīĆū³Ę£© ”£
£Ø2£©ÓÉĀĖŅŗAÖʵĆAlCl3ČÜŅŗÓŠĶ¾¾¶IŗĶ¢ņĮ½Ģõ£¬ÄćČĻĪŖŗĻĄķµÄŹĒ____________”£
Š“³öA¾Ķ¾¾¶¢ņÉś³ÉDµÄĄė×Ó·½³ĢŹ½ ”£
£Ø3£©“ÓĀĖŅŗEÖŠĮņĖįµĆµ½ĀĢ·Æ¾§ĢåµÄŹµŃé²Ł×÷ŹĒ ”£
£Ø4£©Š“³öÓĆĀĖŌüFÖʱøCuSO4ČÜŅŗµÄ»Æѧ·½³ĢŹ½£ØŅŖĒó½ŚŌ¼£¬»·±££©
£Ø5£©ÓŠĶ¬Ń§Ģį³öæɽ«·½°øÖŠ×ī³õČܽāŗĻ½šµÄÉÕ¼īøÄÓĆŃĪĖį£¬ÖŲŠĀÉč¼Ę·½°ø£¬Ņ²ÄÜÖʵĆČżÖÖĪļÖŹ£¬ÄćČĻĪŖŗóÕߵķ½°øŹĒ·ńøüŗĻĄķ £¬ĄķÓÉŹĒ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģɽ¶«Ź”µĀÖŻŹŠøßČż10ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ļņl mL 0.5mol”¤L£1AlCl3ČÜŅŗÖŠ¼ÓČė3 mL±„ŗĶNaFČÜŅŗ£¬ŌŁ¼ÓČėl mL 3mol”¤L£1°±Ė®£¬Ć»ÓŠÉś³É°×É«³Įµķ£¬Ęä×īÖ÷ŅŖµÄŌŅņŹĒ
A£®3mol”¤L£1°±Ė®µÄÅØ¶Č²»¹»“ó£¬ČÜŅŗµÄ¼īŠŌ²»¹»Ēæ
B£®NaFČÜŅŗ¼īŠŌ½ĻĒ棬Al3+ĶźČ«·“Ӧɜ³ÉAlO2££¬¶ųAlO2£²»ÄÜÓė°±Ė®·“Ӧɜ³ÉAl(OH)3
C£®°±Ė®ĪŖČõ¼īČÜŅŗ£¬Al3+²»ÓėČõ¼ī·“Ó¦
D£®Al3+ÓėF£½įŗĻÉś³ÉŠĀĪļÖŹ£¬ČÜŅŗÖŠ¼øŗõƻӊAl3+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģɽ¶«Ź”øßČżÉĻѧʌµŚŅ»“ĪÄ£Äāæ¼ŹŌŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŹµŃéĢā
(8·Ö)ĀĮŹĒŅ»ÖÖÖŲŅŖµÄ½šŹō£¬ŌŚÉś²ś”¢Éś»īÖŠ¾ßÓŠŠķ¶ąÖŲŅŖµÄÓĆĶ¾£¬ĻĀĶ¼ŹĒ“ÓĀĮŹææóÖŠÖʱøĀĮµÄ¹¤ŅÕĮ÷³Ģ£ŗ
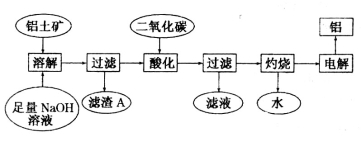
ŅŃÖŖ£ŗ
£Ø1£©ĀĮĶĮæóµÄÖ÷ŅŖ³É·ÖŹĒAl2O3£¬“ĖĶā»¹ŗ¬ÓŠÉŁĮæSiO2”¢Fe2O3µČŌÓÖŹ£»
£Ø2£©ČÜŅŗÖŠµÄNa2SiO3ÓėNa[A1(OH)4]·“Ó¦£¬ÄÜÉś³É¹čĀĮĖįŃĪ³Įµķ£¬»Æѧ·“Ó¦·½³ĢŹ½ĪŖ£ŗ
2Na2SiO3+2Na[A1(OH)4]==Na2A12Si2O8”ż+2H2O+4NaOH
»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öĻņĀĮĶĮæóÖŠ¼ÓČė×ćĮæĒāŃõ»ÆÄĘČÜŅŗŗó£¬øĆ²½²Ł×÷ÖŠÖ÷ŅŖ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½£ŗ
___________________________________Ӣ__________________________________ӣ
£Ø2£©ĀĖŌüAµÄÖ÷ŅŖ³É·ÖĪŖ___________£»ĀĖŌüAµÄÓĆĶ¾ŹĒ(Ö»Š“Ņ»ÖÖ)___________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015½ģɽ¶«Ź”øßČż11ŌĀ½×¶ĪÄ£æéæ¼ŹŌ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
”°»ÆѧŹĒŅ»ĆÅÖŠŠÄѧæĘ£¬ÓėÉē»į”¢Éś»ī”¢æĘŃŠĆÜĒŠµÄ¹ŲĻµ”±”£ĻĀĮŠŠšŹöÖŠ£¬²»ÕżČ·µÄŹĒ
A£®“óĮæŹ¹ÓĆČ¼Ćŗ·¢µēŹĒŠĪ³ÉĪķö²µÄÖ÷ŅŖŌŅņ
B£®ĢģČ»Ęų”¢ĆŗĘų“óĮ抹Ā©Óöµ½Ć÷»š»į±¬ÕØ
C£®ĄūÓĆ»Æѧ·“Ó¦æÉŹµĻÖ12Cµ½14CµÄ×Ŗ»Æ
D£®¾§Ģå¹čæÉÓĆÓŚ¹ā·ü·¢µē”¢ÖĘŌģŠ¾Ę¬
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com