
| A.福尔马林(蚁酸):加入足量饱和碳酸钠溶液充分振荡,蒸馏,收集馏出物 |
| B.乙醇(水):加入足量生石灰,蒸馏,收集馏出物 |
| C.苯(苯酚):加溴水,振荡,过滤除去沉淀 |
| D.乙酸乙酯(乙酸):加饱和碳酸钠溶液,充分振荡,分液,弃水层 |
科目:高中化学 来源:不详 题型:单选题
| A.应使混合物中的水分完全蒸干后,才能停止加热 |
| B.蒸馏操作时,应使温度计水银球靠近蒸馏烧瓶的支管口处 |
| C.分液操作时,下层液体从分液漏斗下口放出后再将上层液体从下口放出到另一个烧杯中 |
| D.萃取操作时,应选择有机萃取剂,且萃取剂的密度必须比水大 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用氢气除去乙烷中混有的少量乙烯 |
| B.用金属钠除去乙醇中混有的少量水 |
| C.用酸性高锰酸钾溶液除去甲烷中混有的少量乙烯 |
| D.用饱和碳酸氢钠溶液除去二氧化碳中混有的少量氯化氢 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| 选项 | 混合物 | 试剂 | 分离方法 |
| A. | 溴乙烷(乙醇) | 生石灰 | 蒸馏 |
| B. | 甲烷(乙烯) | 酸性高锰酸钾溶液 | 洗气 |
| C. | 苯(硝基苯) | 蒸馏水 | 分液 |
| D. | 苯甲酸(NaCl) | 蒸馏水 | 重结晶 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
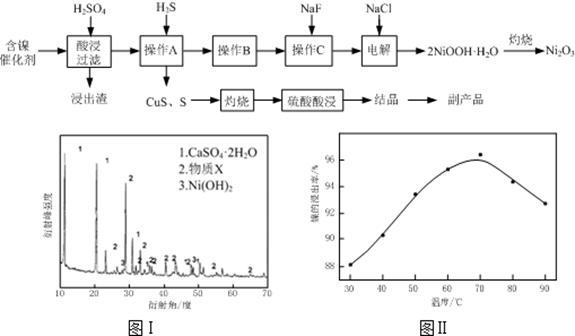
| 氢氧化物 | Fe(OH)3 | Fe(OH)2 | Ni(OH)2 |
| 开始沉淀的pH | 1.5 | 6.5 | 7.7 |
| 沉淀完全的pH | 3.7 | 9.7 | 9.2 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.用KOH溶液鉴别SO3(g)和SO2 |
| B.用湿润碘化钾淀粉试纸鉴别Br2(g)和NO2 |
| C.用CO2鉴别NaAlO2溶液和CH3COONa溶液 |
| D.用BCl2溶液鉴别AgNO3溶液和K2SO4溶液 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com