

图3
(1)FexO中x值(精确至0.01)为___________________。
(2)晶体中的Fen+分别为Fe2+、Fe3+,在Fe2+和Fe3+的总数中,Fe2+所占分数(用小数表示,精确至0.001)为_______________。
(3)此晶体化学式为_________________。
(4)与某个Fe2+(或Fe3+)距离最近且等距离的O2-围成的空间几何形状是_______________。
(5)在晶体中,铁元素的离子间最短距离为___________m。
解析:(1)根据NaCl晶体结构,1个NaCl晶胞是由8个小立方体〔如图(1)〕构成的。每个小立方体为![]() NaCl,同理在FexO晶体中,每个小立方体为
NaCl,同理在FexO晶体中,每个小立方体为![]() 个FexO,完整晶体中〔如图(2)〕Fe、O交替出现,x=1。
个FexO,完整晶体中〔如图(2)〕Fe、O交替出现,x=1。

(1)每个小立方体的质量为:
m=ρV=![]() )3=5.60×10
)3=5.60×10
M(FexO)=
x=0.92
(2)设1 mol Fe0.92O中,n(Fe2+)=y mol,则:n(Fe3+)=(0.92-y)mol。根据化合物中各元素正负化合价代数和为零的原则:2×y mol+3×(0.92 mol-y mol)+(-2)×1 mol=0
y=0.76
故Fe2+所占分数为0.76/0.92=0.826。
(3)由于Fe2+为0.76,则Fe3+为0.92-0.76=0.16,故化学式为![]() O。
O。
(4)Fe在晶体中所占空隙的几何形状为正八面体。如图(3)所示。
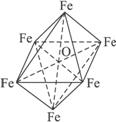
图(3)
(5)如图(1),铁元素离子间的距离
r=![]() =1.41×4.28×10
=1.41×4.28×10![]() =3.02×10
=3.02×10
答案:(1)0.92 (2)0.826 (3)![]() O
O
(4)见图(3) (5)3.02×10-10 m


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源:吉林省长春外国语学校2011-2012学年高二下学期期末考试化学试题 题型:022
(1)熔点沸点HF________HI;原因:________.
(2)各种含氧酸HClO、HClO3、H2SO3、HClO4的酸性由强到弱排列为________.
(3)下列4种物质熔点沸点由高到低排列为________(填序号).
①金刚石(C-C)②锗(Ge-Ge)
③晶体硅(Si-Si)④金刚砂(Si-C)
(4)晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞.NaCl晶体结构如下图所示.晶体中每个Na+同时吸引着________个Cl-,由这些Cl-构成的几何构型为________晶体中在每个Cl-周围与它最接近且距离相等的Cl-共有________个.

(5)某元素的激发态原子的电子排布式为1s22s22p63s23p34s1,则该元素基态原子的电子排布式为________;其最高价氧化物对应的水化物的化学式是________.
(6)某元素原子的价电子构型为3d104S2,它属于第________周期,是________族,________区元素,元素符号是________.该原子核外有________个能级,电子云的形状有________种.
查看答案和解析>>
科目:高中化学 来源:2011-2012学年吉林省长春外国语学校高二下学期期末考试化学试卷(带解析) 题型:填空题
(1)、熔点沸点HF HI;原因:
(2)、各种含氧酸HClO、HClO3、H2SO3、HClO4的酸性由强到弱排列为
(3)、下列4种物质熔点沸点由高到低排列为________ (填序号)
①金刚石(C—C)②锗(Ge—Ge)
③晶体硅(Si—Si)④金刚砂(Si—C)
(4)晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞。NaCl晶体结构如图所示。
晶体中每个Na+同时吸引着______个Cl-,由这些 Cl-构成的几何构型为 晶体中在每个Cl-周围与它最接近且距离相等的Cl-共有________个。
(5)某元素的激发态原子的电子排布式为1s 2s
2s 2p
2p 3s
3s 3p
3p 4s
4s ,则该元素基态原子的电子排布式为 ;其最高价氧化物对应的水化物的化学式是
,则该元素基态原子的电子排布式为 ;其最高价氧化物对应的水化物的化学式是
(6)某元素原子的价电子构型为3d104S2,它属于第 周期,是 族, 区元素,元素符号是 。该原子核外有 个能级,电子云的形状有 种
查看答案和解析>>
科目:高中化学 来源:2013届吉林省高二下学期期末考试化学试卷(解析版) 题型:填空题
(1)、熔点沸点HF HI;原因:
(2)、各种含氧酸HClO、HClO3、H2SO3、HClO4的酸性由强到弱排列为
(3)、下列4种物质熔点沸点由高到低排列为________ (填序号)
①金刚石(C—C)②锗(Ge—Ge)
③晶体硅(Si—Si)④金刚砂(Si—C)
(4)晶体具有规则的几何外形,晶体中最基本的重复单元称之为晶胞。NaCl晶体结构如图所示。

晶体中每个Na+同时吸引着______个Cl-,由这些 Cl-构成的几何构型为 晶体中在每个Cl-周围与它最接近且距离相 等的Cl-共有________个。
(5)某元素的激发态原子的电子排布式为1s 2s
2s 2p
2p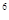 3s
3s 3p
3p 4s
4s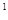 ,则该元素基态原子的电子排布式为
;其最高价氧化物对应的水化物的化学式是
,则该元素基态原子的电子排布式为
;其最高价氧化物对应的水化物的化学式是
(6)某元素原子的价电子构型为3d104S2,它属于第 周期,是 族, 区元素,元素符号是 。该原子核外有 个能级,电子云的形状有 种
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com