
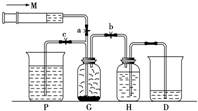
 某课外活动小组利用如图所示的装置制取Cl2,提供的试剂有浓盐酸、饱和食盐水(Cl2在其中溶解度较小)、氢氧化钠溶液、高锰酸钾固体,反应的化学方程式为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O
某课外活动小组利用如图所示的装置制取Cl2,提供的试剂有浓盐酸、饱和食盐水(Cl2在其中溶解度较小)、氢氧化钠溶液、高锰酸钾固体,反应的化学方程式为:2KMnO4+16HCl(浓)=2KCl+2MnCl2+5Cl2↑+8H2O

科目:高中化学 来源: 题型:
| A、△H1>△H2 |
| B、△H1<△H2 |
| C、△H1=△H2 |
| D、无法确定 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某温度下,1LpH=8的纯水中含OH-为10-8NA |
| B、14g分子通式为CnH2n的链烃中含有的C=C键数目为NA |
| C、标准状况下,22.4LCl2与足量Fe反应,转移的电子数为3NA |
| D、常温下,1L0.1mol?L-1CH3COONa溶液中含有的Na+和CH3COO-总数为0.2NA |
查看答案和解析>>
科目:高中化学 来源: 题型:
| (1)草 酸晶体 | 分子式 | H2C2O4?2H2O | 颜色 | 无色晶体 | ||
| 熔点 | 100.1℃ | 受热至100.1℃时失去结晶水,成为无水草酸. | ||||
| (2)无 水草酸 | 结构简式 | HOOC-COOH | 溶解性 | 能溶于水或乙醇 | ||
| 特性 | 大约在157℃升华(175℃以上发生分解). | |||||
| 化学性质 | H2C2O4+Ba(OH)2=BaC2O4↓+2H2O | |||||
HOOC-COOH
| ||||||

查看答案和解析>>
科目:高中化学 来源: 题型:

| B2H6 |
| H2O2/OH |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、SO3的分解率为20% |
| B、10min内用O2表示的该反应的反应速率为0.005mol/(L?min) |
| C、容器内气体的密度为40g/L |
| D、达到平衡时分解的Ag2SO4固体为0.5mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
 )是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
)是其中的一种,它可以从茉莉花中提取,也可以用甲苯和乙醇为原料进行人工合成.一种合成路线如下:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com