
����Ŀ������A��B��C��D��E��F���ֶ���������Ԫ�أ�ԭ����������������֪A����̬�⻯������������������ˮ���ﷴӦ��Bԭ�������������ǵ��Ӳ�����3����C+��D3+���ӵĵ��Ӳ�ṹ��ͬ��B��E����ͬһ���壮
��ش��������⣺
��1��E��Ԫ�����ڱ��е�λ����
��2������Ԫ���γɵļ������У��뾶��С�����������ӷ��ţ���
��3��������Ԫ���е�һ�ֻ�����ɵ����ʼ��Է�����ͼ1��Ӧ��
�����Ҿ���Ư���ԣ����ҵĵ���ʽΪ ��
��������ˮ��Һ��ǿ������Һ�����Ϊ�����ѧʽ����
������Ϊ��Ԫ���ᣬ����������ǿ�ᡢ��������ǿ����ҵ�����Ϊ���õ��뷽��ʽ��ʾ����������ǿ�ᡢ��������ǿ���ԭ�� ��
������������Ϊ����ɫ����ͬѧ��Ϊ��Ũ������Ը�������ס���Ϊ��֤��۵��Ƿ���ȷ������ͼ2װ�ý���ʵ��ʱ����Һ©����Ӧ���������Լ����ƣ���ʵ������У�Ũ������δ�����������ݳ�������Һ��Ϊ����ɫ���ɴ˵ó��Ľ����� ��
���𰸡�
��1���������ڵ�VIA��
��2��Al 3+
��3��![]() ��Na��Na2O2������������AlO2��+H2O+H+?Al��OH��3?Al3++3OH����Ũ���Ũ����ܸ�������������������������Ũ����
��Na��Na2O2������������AlO2��+H2O+H+?Al��OH��3?Al3++3OH����Ũ���Ũ����ܸ�������������������������Ũ����
���������⣺A��B��C��D��E��F���ֶ���������Ԫ�أ�ԭ��������������A����̬�⻯������������������ˮ���ﷴӦ����A��NԪ�أ�
Bԭ�������������ǵ��Ӳ�����3����BΪOԪ�أ�
B��E����ͬһ���壬��E��SԪ�أ�FΪ����������Ԫ����ԭ����������E����FΪClԪ�أ�
C+��D3+���ӵĵ��Ӳ�ṹ��ͬ��Ϊ��������Ԫ�أ�C��D�ֱ�ΪNa��AlԪ�أ���1��E��SԪ�أ�Sԭ�Ӻ�����Ӳ�����������������������������������������Sԭ�Ӻ�����3�����Ӳ㡢������������6������Sλ�ڵ������ڵ�VIA�壬���Դ��ǣ��������ڵ�VIA�壻��2������Ԫ���γɵļ������У����Ӳ���Խ�ٵ�ԭ�Ӱ뾶ԽС�����Ӳ�ṹ��ͬ�����ӣ����Ӱ뾶����ԭ�������������С���⼸��Ԫ���γɵ����Ӱ뾶��С˳����S 2����Cl����N3����O 2����Na+��Al 3+ �� �������Ӱ뾶��С����Al 3+ �� ���Դ��ǣ�Al 3+����3�������Ҿ���Ư���ԣ�ΪHClO�����������������HCl��HClO������Oԭ�Ӻ�H��Clԭ��֮��ֱ���һ�Ե��ӣ�����ʽΪ ![]() �����Դ��ǣ�
�����Դ��ǣ� ![]() ����������ˮ��Һ��ǿ������Һ�����ΪNa��Na2O2 �� ��ΪNaOH����Ϊ���������������Դ��ǣ�Na��Na2O2��������Ϊ��Ԫ���ᣬ����������ǿ�ᡢ��������ǿ���Ϊ������������Ϊ���⣬�����������������Ϊ����������ᣬ���������ܷ�����ʽ����Ҳ�ܷ�����ʽ���룬���뷽��ʽΪAlO2��+H2O+H+Al��OH��3Al3++3OH�� �� ������������������ǿ���ǿ����Һ�����Դ��ǣ�����������AlO2��+H2O+H+Al��OH��3Al3++3OH����������������Ϊ����ɫ������ΪNO����Ϊ������������ͬѧ��Ϊ��Ũ������Ը�������ס���Ϊ��֤��۵��Ƿ���ȷ������ͼ2װ�ý���ʵ��ʱ��Ũ�����Cu��Ӧ���ɶ������������Է�Һ©����Һ����Ũ���ᣬʵ������У�Ũ������δ�����������ݳ�������Һ��Ϊ����ɫ���������������Ũ���ᣬ˵����������������Ũ�����Ũ����ܸ������������
����������ˮ��Һ��ǿ������Һ�����ΪNa��Na2O2 �� ��ΪNaOH����Ϊ���������������Դ��ǣ�Na��Na2O2��������Ϊ��Ԫ���ᣬ����������ǿ�ᡢ��������ǿ���Ϊ������������Ϊ���⣬�����������������Ϊ����������ᣬ���������ܷ�����ʽ����Ҳ�ܷ�����ʽ���룬���뷽��ʽΪAlO2��+H2O+H+Al��OH��3Al3++3OH�� �� ������������������ǿ���ǿ����Һ�����Դ��ǣ�����������AlO2��+H2O+H+Al��OH��3Al3++3OH����������������Ϊ����ɫ������ΪNO����Ϊ������������ͬѧ��Ϊ��Ũ������Ը�������ס���Ϊ��֤��۵��Ƿ���ȷ������ͼ2װ�ý���ʵ��ʱ��Ũ�����Cu��Ӧ���ɶ������������Է�Һ©����Һ����Ũ���ᣬʵ������У�Ũ������δ�����������ݳ�������Һ��Ϊ����ɫ���������������Ũ���ᣬ˵����������������Ũ�����Ũ����ܸ������������
���Դ��ǣ�Ũ���Ũ����ܸ�������������������������Ũ���ᣮ



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����NaCl��������0.1 mol��L-1��NaCl��Һ�����в�����˵����ȷ����
A����5.85gNaCl��������1 Lˮ�п����0.1 mol��L-1��NaCl��Һ
B������ʱ��������NaClֱ�ӷ�����ƽ������
C�������ܽ����Һת�Ƶ�����ƿ�У�Ȼ��������ƿ��ֱ�Ӽ�ˮϡ�͵��̶���
D��������Һʱ����ƿ��ԭ������������ˮ����Ӱ��ʵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ˮ(D2O)����Ҫ�ĺ˹�ҵԭ�ϣ�����˵���������
A. �(D)��ԭ�Ӻ�����1������ B. 1 H��D����ͬλ��
C. H2O��D2O����ͬ�������� D. 1 H218O��D216O����Է���������ͬ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����з���ʽ��ʾ������һ���Ǵ�������ǣ� ��
A.CH4
B.C2H6O
C.C6H12O6
D.C2H4Cl2
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij�о���ѧϰС����Ũ��Ϊ0.20mol��L-1�������Һ�ζ�����һ�������ʵ��ռ���Ʒ(���������Ӧ)����ˮ�γɵ���Һ��
��1��ȷ��ȡһ������Ĵ���Һ��Ҫʹ�õ�������______________��
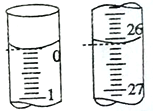
��2�����ζ���ʼ�ͽ���ʱ���ζ����е�Һ����ͼ��ʾ�������������Һ�����Ϊ________mL��
��3���ζ�ʱ�����Է�̪Ϊָʾ�����ζ��ﵽ�յ�ı�־��______________________________��
��4����ȷ��ȡ��5.0g�ռ���Ʒ���Ƴ�250mL����Һ�����������Һ�ζ����ζ�ǰ�������ζ���������±���ʾ��
�ζ����� | ����Һ���(mL) | 0.20mol��L-1���������(mL) | |
�ζ�ǰ���� | �ζ������ | ||
��һ�� | 10.00 | 0.70 | 20. 60 |
��һ�� | 10.00 | 4.00 | 24.10 |
������ | 10.00 | 1.10 | 21.10 |
��ʵ�����ݿ�֪���ռ�Ĵ���Ϊ__________��
��5�����в����ᵼ�²�õĴ���Һ��Ũ��ƫ�����________(����ĸ)��
a.���ֱ�Һ�γ���ƿ�� b.�ô�����Һ��ϴ��ƿ
C.��ƿϴ������������ˮ d.�ų���Һ�ĵζ��ܿ�ʼ�����ݣ��ų�Һ���������ʧ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ʹһþ���Ͻ��ĩ�ڹ���ϡH2SO4���ܽ⣬��������Һ�м���NaOH��Һ�����ɳ���������w�ͼ���NaOH��Һ�����V�Ĺ�ϵ��ͼ��ʾ����úϽ���þ����������֮��Ϊ�� �� 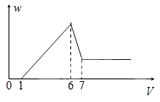
A.2��3
B.1��1
C.4��3
D.8��9
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����б仯�У��ɼӳɷ�Ӧ�������
A. ��ϩͨ�����Ը��������Һ�У����������Һ��ɫ
B. ��̼ԭ�ӽ϶���������ȡ���ѹ�����������·�Ӧ���ɺ�̼ԭ�ӽ��ٵ�������ϩ��
C. �ڹ��������£�C2H6��Cl2��Ӧ��������״Һ��
D. �ڴ��������£� ��ϩ��ˮ��Ӧ�����Ҵ�
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ijͬѧ��һ��ɫ����Һ���з����ó�����Һ�к�������ij�����ӣ�����Ϊ��������Ӧ����
A��Al3+��NO3�D��K+��SO42�� B��Ca2+��H+��CO32����AlO2�D
C��OH����SO42����NH4+��Al3+ D��Fe3+��Mg2+��NO3����Cl��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪A��B��D��H����ѧ��ѧ�г����ĵ��ʣ�JΪ��ɫ��Һ��ת����ϵ���£����������P��Ӧ��������ȥ����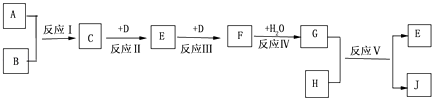
��1����A��B��Ϊ����ʱ�����ò������ֱ�պȡC��G��Ũ��Һ��ʹ���ǿ���ʱ���а������ɣ���
����д���������ʵĻ�ѧʽD �� E ��
����д����Ӧ��Ļ�ѧ����ʽ
��2����AΪ���壬BΪ����ʱ����֪C��D����ȫȼ�տ�����E��ˮ��E��һ�ֳ����Ŀ�����Ⱦ��ҽ�C��E��Ͽ����ɵ���ɫ����B��д��C��E��Ӧ�Ļ�ѧ����ʽ��������������E�ķ��� ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com