
NaOH标准溶液的配制和标定,需经过NaOH溶液配制、基准物质H2C2O4?2H2O的称量以及用NaOH溶液滴定等操作。下列有关说法正确的是

A.用图甲所示操作转移NaOH溶液到容量瓶中
B.用图乙所示装置准确称得0.1575gH2C2O4?2H2O固体
C.用图丙所示操作排除碱式滴定管中的气泡
D.用图丁所示装置以NaOH待测液滴定H2C2O4溶液
 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案科目:高中化学 来源:2014-2015学年四川省广安市高三“一诊”理综化学试卷(解析版) 题型:填空题
(14分)在某温度下、容积均为2L的三个密闭容器中,按不同方式投入反应物,保持恒温恒容,使之发生反应:2 H2(g)+CO(g) CH3OH(g);
CH3OH(g);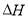 =-a KJ·mol-1(a>0)。初始投料与各容器达到平衡时的有关数据如下:
=-a KJ·mol-1(a>0)。初始投料与各容器达到平衡时的有关数据如下:
(1)该温度下此反应反应物的总键能和 (填“大于”“等于”或“小于”)生成物的总键能和。
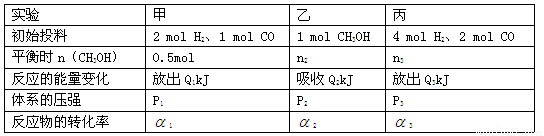
(2)在该温度下,假设甲容器从反应开始到平衡所需时间为4 min,则H2的平均反应速率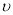 ( H2)为 。
( H2)为 。
(3)下列选项能说明甲容器中的反应已经达到平衡状态的有 (填序号)。
A.容器内H2、CO、CH3OH的物质的量之比为2:1:1
B.容器内气体的密度保持恒定
C.容器内H2气体的体积分数保持恒定
D.2V正(H2)=V逆(CO)
(4)丙容器中,平衡后将容器的容积压缩到原来的l/2,其他条件不变,对平衡体系产生的影响是
(填字母序号)。
A.c(H2)减少
B.正反应速率加快,逆反应速率减慢
C.CH3OH 的物质的量增加
D.重新平衡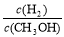 减小
减小
E.平衡常数K增大
(5)三个容器中的反应分别达平衡时各组数据关系正确的是 (填序号)。
A.Q1+Q2=a B.α3<α1
C.P3<2P1=2P2 D.n2<n3<1.0mol
(6)已知:①3CO(g) +3H2(g) CH3OCH3(g) +CO2(g) △H=—247kJ·mol-l
CH3OCH3(g) +CO2(g) △H=—247kJ·mol-l
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H= -24 kJ·mol-l
CH3OCH3(g)+H2O(g) △H= -24 kJ·mol-l
③CO(g)+H2O(g) CO2(g)+H2(g) △H= -41 kJ·mol-l
CO2(g)+H2(g) △H= -41 kJ·mol-l
2 H2(g)+CO(g) CH3OH(g);
CH3OH(g);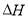 =-a KJ·mol-1 ,则 a=
=-a KJ·mol-1 ,则 a=
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省高三质量检测化学试卷(解析版) 题型:选择题
新型纤维酸类降脂药克利贝特可由物质X在一定条件下反应制得:
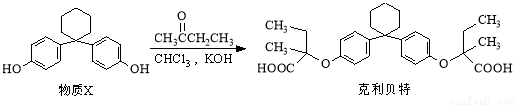
下列有关叙述正确的是
A.克利贝特的分子式为C28H34O6
B.物质X分子中所有碳原子可能位于同一平面内
C.用饱和NaHCO3溶液可以鉴别物质X和克利贝特
D.1 mol物质X最多可以与含2 molBr2的溴水反应
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:推断题
(15分)己烯雌酚(stilbestrol)是非甾体雌激素物质,可通过以下方法合成
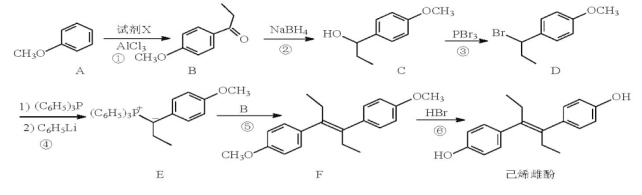
(1)化合物B中的含氧官能团为 和 (填名称)。
(2)反应①中加入的试剂X的分子式为C3H5ClO,X的结构简式为 。
(3)上述反应①②③⑥中,属于取代反应的是 (填序号)。
(4)B的一种同分异构体满足下列条件:
I、能发生银镜反应,其水解产物之一能与FeCl3溶液发生显色反应。
II、分子中有4种不同化学环境的氢。
写出该同分异构体的结构简式: (任写一种)。
(5)根据已有知识并结合相关信息,写出以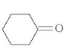 为原料制备
为原料制备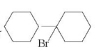 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:

查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省南京市、盐城市高三一模化学试卷(解析版) 题型:选择题
己知:
①2H2(g)+O2(g) 2H2O(g)△H1
2H2O(g)△H1
②H2(g)+Cl2(g) 2HCl(g)△H2
2HCl(g)△H2
③4H Cl (g)+O2(g) 2 Cl2(g)+2H2O(g)△H3
2 Cl2(g)+2H2O(g)△H3
④N2(g)+3H2(g) 2NH3(g)△H4
2NH3(g)△H4
⑤2NH3(g)+3 Cl2(g) N2(g)+6HCl(g)△H5
N2(g)+6HCl(g)△H5
下列关于上述反应焓变的判断正确的是
A.△H1>0,△H2>0 B.△H3>0,△H4>0
C.△H2=△H4+△H5 D.△H3=△H1-2△H2
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港等四市高三一模化学试卷(解析版) 题型:实验题
《化学实验》邻苯二甲酸二异癸酯为无色粘稠液体,密度约为0.966g·cm-3,不溶于水,易溶于有机溶剂,常用作耐热塑料增塑剂。某实验小组的同学用下图所示装置制取少量邻苯二甲酸二异癸酯(图中夹持和加热装置已略去),主要操作步骤如下:
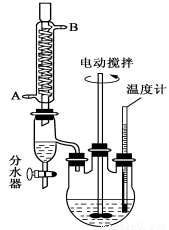
①向三颈烧瓶内加入0.05g钛酸四异丙酯、95.7g异癸醇及37.3g邻苯二甲酸酐;
②搅拌,升温至210℃,持续搅拌反应3小时;
③冷却至室温,将反应混合物倒出,抽滤;
④滤液用饱和碳酸氢钠洗涤、分液,再用蒸馏水洗涤、分液,得到粗产品;
⑤将粗产品加入蒸馏装置,减压蒸馏,获得成品。
请回答下列问题:
(1)加入钛酸四异丙酯的作用为 。
(2)步骤②中升温至210℃,持续搅拌反应3小时的目的是 ;
判断反应已结束的方法是 。
(3)步骤③抽滤时用到的硅酸盐质仪器有 、 。
(4)步骤④中分液时,得到粗产品的实验操作为 。
(5)步骤⑤中减压蒸馏的目的是 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏省连云港等四市高三一模化学试卷(解析版) 题型:选择题
恒温恒容下,向2L密闭容器中加入MgSO4(s)和CO(g),发生反应:
MgSO4(s)+CO(g) MgO(s)+CO2(g)+SO2(g),反应过程中测定的部分数据见下表:
MgO(s)+CO2(g)+SO2(g),反应过程中测定的部分数据见下表:
反应时间/min | n(MgSO4)/mol | n(CO)/mol | n(CO2) / mol |
0 | 2.00 | 2.00 | 0 |
2 | 0.80 | ||
4 | 1.20 |
下列说法正确的是
A.反应在0~2min内的平均速率为v(SO2)=0.6 mol·L-1·min-1
B.反应在2~4min内容器内气体的密度没有变化
C.若升高温度,反应的平衡常数变为1.00,则正反应为放热反应
D.保持其他条件不变,起始时向容器中充入1.00mol MgSO4和1.00molCO,到达平衡时n(CO2)>0.60mol
查看答案和解析>>
科目:高中化学 来源:2014-2015学年江苏常州市高三第一次调研试卷化学试卷(解析版) 题型:实验题
(15分)三草酸合铁(Ⅲ)酸钾晶体(K3[Fe(C2O4)3]·3H2O)有很重要的用途。可用如下流程来制备。根据题意完成下列各题:
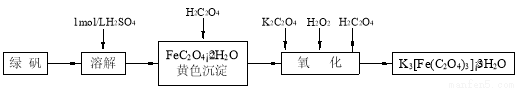
(1)若用铁和稀硫酸制备绿矾(FeSO4·7H2O)过程中,其中 (填物质名称)往往要过量,理由是 。
(2)要从溶液中得到绿矾,必须进行的实验操作是 。(按前后顺序填)
a.过滤洗涤
b.蒸发浓缩
c.冷却结晶
d.灼烧
e.干燥
某兴趣小组为测定三草酸合铁酸钾晶体(K3[Fe(C2O4)3]·3H2O)中铁元素含量,做了如下实验:
步骤1:称量5.000g三草酸合铁酸钾晶体,配制成250ml溶液。
步骤2:取所配溶液25.00ml于锥形瓶中,加稀H2SO4酸化,滴加KMnO4溶液至草酸根恰好全部被氧化成二氧化碳,同时,MnO4— 被还原成Mn2+。向反应后的溶液中加入一定量锌粉,加热至黄色刚好消失,过滤,洗涤,将过滤及洗涤所得溶液收集到锥形瓶中,此时,溶液仍显酸性。
步骤3:在酸性条件下,用0.010mol/L KMnO4溶液滴定步骤二所得溶液至终点,共做三次实验,平均消耗KMnO4溶液20.00mL,滴定中MnO4-,被还原成Mn2+。
(3)步骤1中,配制三草酸合铁酸钾溶液需要使用的玻璃仪器除烧杯、玻璃棒以外还有 ;主要操作步骤依次是:称量、溶解、转移、 、定容、摇匀。
(4)步骤2中,加入锌粉的目的是 。
(5)步骤3中,发生反应的离子方程式为 。
(6)步骤2中,若加入的KMnO4的溶液的量不够,则测得的铁含量 。(选填“偏低”、“偏高”、“不变”)
(7)某同学将8.74g无水三草酸合铁酸钾(K3[Fe(C2O4)3])在一定条件下加热分解,所得固体的质量为5.42g,同时得到密度为1.647g/L(已折合成标准状况下)气体。研究固体产物得知,铁元素不可能以三价形式存在,而盐只有K2CO3。写出该分解反应的化学方程式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年广东省深圳市高三第一次调研考试理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数。下列说法正确的是
A.20g重水(2H2O)含有的中子数为10 NA
B.常温常压下,7.1g Cl2完全溶于水转移电子数为0.1NA
C.标准状况下,2.24L CCl4中含有C—Cl键数为0.4NA
D.1 mol·L-1 FeCl3溶液含有的Cl-数为3NA
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com