
| A、石灰石 | B、纯碱 | C、石英 | D、黏土 |
 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案 综合自测系列答案
综合自测系列答案科目:高中化学 来源: 题型:
| 元素编号 | 元素性质或原子结构 |
| T | 单质能与水剧烈反应,所得溶液呈弱酸性 |
| X | L层p电子数比s电子数多2个 |
| Y | 第3周期元素的简单离子中半径最小 |
| Z | L层有三个未成对电子 |
查看答案和解析>>
科目:高中化学 来源: 题型:
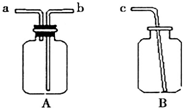 化学是一门以实验为基础的科学.
化学是一门以实验为基础的科学.查看答案和解析>>
科目:高中化学 来源: 题型:
| A、发烟硫酸的摩尔质量为178 |
| B、反应①中氧化剂与还原剂的物质的量之比为2:3 |
| C、反应②中氧化产物与还原产物的物质的量之比为1:3 |
| D、若反应②中消耗2 mol I2(SO4)3,则电子转移3 mol |
查看答案和解析>>
科目:高中化学 来源: 题型:
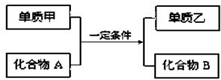 置换反应的通式可表示为如图:单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:
置换反应的通式可表示为如图:单质甲、乙和化合物A、B为中学常见物质,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、CO2 能使漂白粉水溶液先变浑浊后变澄清,SO2 也有同样现象 |
| B、加热条件下,Na与O2 反应生成Na2O2,Li与O2反应也声称Li2O2 |
| C、常温下,浓硝酸能使铁、铝钝化,浓硫酸也能使铁、铝钝化 |
| D、氯气可置换出KI溶液中的碘,氟气也可置换出KI溶液中的碘 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、新制氯水显酸性,向其中滴加少量紫色石蕊试液,充分振荡后溶液呈红色 |
| B、加水稀释溶液,溶液中的所有离子浓度都减小 |
| C、金属铝的生产是以Al2O3为原料,在熔融状态下进行电解 |
| D、NaHCO3溶液中含有少量Na2CO3可以用澄清石灰水除去 |
查看答案和解析>>
科目:高中化学 来源: 题型:
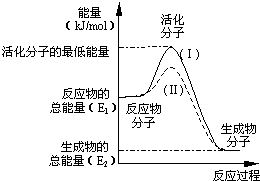 在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题.
在化学反应中,只有极少数能量比平均能量高得多的反应物分子发生碰撞时才可能发生化学反应,这些分子称为活化分子,使普通分子变成活化分子所需提供的最低限度的能量叫活化能,其单位通常用kJ/mol表示.请认真观察如图,然后回答问题.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com