
 有机物A的结构简式为
有机物A的结构简式为 ,它可通过不同化学反应分别制得B、C和D三种物质.
,它可通过不同化学反应分别制得B、C和D三种物质.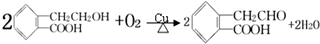 ,
,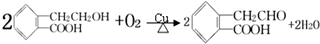 ;
; ,
, .
.


 快乐5加2金卷系列答案
快乐5加2金卷系列答案科目:高中化学 来源: 题型:
| ||
| A、该反应中镁发生了氧化反应 |
| B、该反应中二氧化碳是还原剂 |
| C、该反应属于置换反应 |
| D、镁着火时不能用二氧化碳灭火剂扑灭 |
查看答案和解析>>
科目:高中化学 来源: 题型:

| CO | H2 | CH3OH |
| 2mol | 3mol | 1.0mol |

查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、溶液中Pb2+和I-浓度都增大 |
| B、溶度积常数Ksp不变 |
| C、沉淀溶解平衡不移动 |
| D、溶液中Pb2+和I-浓度不变 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、反应后溶液中Cu2+与Fe2+的物质的量之比为1:2 |
| B、氧化性:Ag+>Cu2+>Fe3+>Zn2+ |
| C、含Fe3+的溶液可腐蚀铜板 |
| D、1mol Fe可还原2mol Fe3+ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com