
根据碘与氢气反应的热化学方程式
①I2(g)+H2(g) 2HI(g)△H=-9.48kJ/mol
2HI(g)△H=-9.48kJ/mol
②I2(s)+H2(g) 2HI(g)△H=+26.48kJ/mol
2HI(g)△H=+26.48kJ/mol
下列判断正确的是
A.254g I2(g)中通入2gH2(g),反应放热9.48 kJ
B.1 mol固态碘与1 mol气态碘所含的能量相差17.00 kJ
C.反应(i)的产物比反应(ii)的产物稳定
D.反应(ii)的反应物总能量比反应(i)的反应物总能量低
科目:高中化学 来源: 题型:
下列关于电离平衡常数(K)的说法正确的是
A.不同浓度的同一弱电解质,其电离平衡常数(K)不同
B.电离平衡常数(K)越小,表示弱电解质电离能力越弱
C.多元弱酸各步电离平衡常数相互关系为:K1<K2<K3
D.CH3COOH溶液中加入少量CH3COONa溶液,电离常数减小
查看答案和解析>>
科目:高中化学 来源: 题型:
下列离子方程式书写正确的是
A. 亚硫酸钠溶液加入稀硝酸:SO32-+2H+= SO2↑+H2O
B.碘水中通入足量的SO2:I2 +SO2+2H2O=2I-+SO42-+4H+
C.NaHSO4溶液与Ba(OH)2溶液反应至中性:H++SO42-+Ba2++OH-=BaSO4↓+H2O
D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4:
3ClO-+2Fe(OH)3=2FeO42-+3Cl-+H2O+4H+
查看答案和解析>>
科目:高中化学 来源: 题型:
化学与生活、生产密切相关,下列说法正确的是
A.碳酸钡、碳酸氢钠、氢氧化铝均可作为抗酸药物使用
B.人体内的蛋白质不断分解,最终生成水和二氧化碳排出体外
C.工业生产玻璃和水泥,均需要用纯碱为原料
D.“地沟油”的主要成分是油脂,其组成与汽油、煤油不相同
查看答案和解析>>
科目:高中化学 来源: 题型:
银质器皿日久表面会逐渐变黑,这是生成了Ag2S的缘故。根据电化学原理可进行如下处理:在铝质容器中加入食盐溶液,再将变黑的银器漫入该溶液中,一段时间后发现黑色会褪去。下列说法正确的是
A.处理过程中银器一直保持恒重
B.银器为正极,Ag2S被还原生成单质银
C.该过程中总反应为2Al+3Ag2S=6Ag+A12S3
D.黑色褪去的原因是黑色Ag2S转化为白色AgC1
查看答案和解析>>
科目:高中化学 来源: 题型:
向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化如图所示。已知: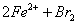 ==2Fe3++2Br-、2Fe3++2I-==2Fe2++I2,下列说法中错误的是
==2Fe3++2Br-、2Fe3++2I-==2Fe2++I2,下列说法中错误的是
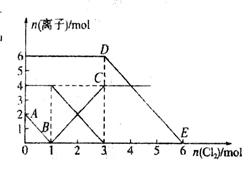
A.还原性:I->Fe2+>Br-
B.线段AB表示Fe2+被氯气氧化
C.线段BC表示生成4 mol Fe3+
D.原溶液中n (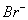 )=6 mol
)=6 mol
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是某化学兴趣小组设计的利用电子垃圾(含70%Cu、25%Al、4%Fe及少量Au、Pt)制备硫酸铜和硫酸铝晶体的路线:
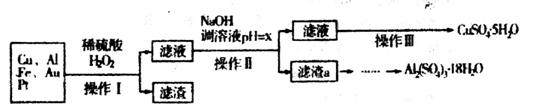
已知下列信息:Cu可与稀硫酸和H2O2的混合液反应生成硫酸铜;铁、铝、铜等离子以氢氧化物形式沉淀时溶液的pH如下表:
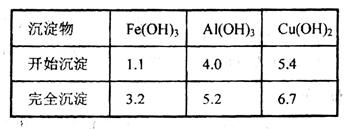
请回答下列问题:
(1)写出Cu与稀硫酸和H2O2的混合液反应的化学方程式______________。
(2)在操作II中,x的取值范围是___________________。
(3)在操作III中,蒸发浓缩需要的玻璃仪器有______________________________________。
(4)由滤渣a制取Al2(SO4)3•18H2O,探究小组设计了三种方案:
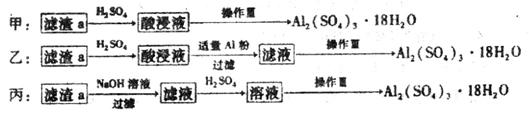
综合考虑上述三种方案,最具可行性的是___________(填序号)。
(5)为测定CuSO4•5H2O晶体的纯度,进行下列实验:取a g 试样配成100mL溶液,每次取20.00mL,消除干扰离子后,用b mol/LEDTA(Na2H2Y)标准溶液滴定其中的Cu2+(离子方程式为Cu2++H2Y2-=CuY2-+2H+),滴定至终点,平均消耗EDTA溶液12.00mL,CuSO4•5H2O晶体的纯度是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
NH3经一系列反应可以得到HNO3,如下图所示。

(1)I中,NH3 和O2在催化剂作用下反应,其化学方程式是_____________________。
(2)II中,2NO(g)+O2 2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如右图)。
2NO2(g)。在其他条件相同时,分别测得NO的平衡转化率在不同压强(P1、P2)下温度变化的曲线(如右图)。

①比较P1、P2的大小关系:________________。
②随温度升高,该反应平衡常数变化的趋势是________________。
③ H ______0
H ______0
(3) I中生成NO 在汽车尾气中可以产生。①已知气缸中生成NO的反应为:
N2(g)+O2(g)  2NO(g)
2NO(g)  H>0;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是________________。
H>0;汽车启动后,气缸温度越高,单位时间内NO排放量越大,原因是________________。
②汽车燃油不完全燃烧时产生CO,有人设想按下列反应除去CO:
2CO(g)=2C(s)+O2(g)已知该反应的 H>0,简述该设想能否实现的依据________________。
H>0,简述该设想能否实现的依据________________。
(4)III中,将NO2( )转化为N2O4(
)转化为N2O4( ),再制备浓硝酸。
),再制备浓硝酸。
①已知:2NO2( )
) N2O4(
N2O4( )△H;当温度升高时,气体颜色变深,则反应为 _____________(填“吸热”或“放热”)反应。
)△H;当温度升高时,气体颜色变深,则反应为 _____________(填“吸热”或“放热”)反应。
②一定温度下,反应(II)的焓变为△H。现将1molN2O4充入一恒容密闭容器中,下列示意图正确且能说明反应达到平衡状态的是 。


(5)IV中,电解NO制备 NH4NO3,其工作原理如右图所示,为使电解产物全部转化为NH4NO3,需补充物质A,A是_____________, 阴极的电极反应______________________________________, 。

查看答案和解析>>
科目:高中化学 来源: 题型:
下列可用来区别SO2和CO2气体的是( )
①澄清的石灰水②氢硫酸③氯水④酸性高锰酸钾⑤氯化钡⑥品红溶液
| A.①④⑤⑥ | B.②③④⑤ | C.①②③⑥ | D.②③④⑥ |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com