
【题目】已知酸性: ![]() >H2CO3>
>H2CO3> ![]() ,综合考虑反应物的转化率和原料成本等因素,将
,综合考虑反应物的转化率和原料成本等因素,将 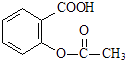 转变为
转变为 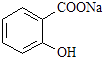 的最佳方法是( )
的最佳方法是( )
A.与稀H2SO4共热后,加入足量的NaOH溶液
B.与稀H2SO4共热后,加入足量的NaHCO3溶液
C.与足量的NaOH溶液共热后,再通入足量CO2
D.与足量的NaOH溶液共热后,再加入适量H2SO4
科目:高中化学 来源: 题型:
【题目】用稀盐酸与稀NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量可计算中和热.回答下列问题: 
(1)该图中有两处未画出,它们是烧杯上方的泡沫塑料盖和 . 泡沫塑料的作用是 .
(2)若NaOH溶液用相同浓度和体积的下列溶液代替,则对中和热数值测定结果将如何影响(填“偏大”、“偏小”、“无影响”):KOH溶液;氨水(NH3H2O) .
(3)某研究小组将V1 mL 1.0mol/L HCl溶液和V2 mL未知浓度的NaOH溶液混合均匀后测量并记录溶液温度,实验结果如图所示(实验中始终保持V1+V2=50mL).由题干及图形可知,V1:V2=时,酸碱恰好完全中和,此反应所用NaOH溶液的浓度应为mol/L.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】利用化学原理可以对工厂排放的废水、废渣等进行有效检测.某工厂对制铬工业污泥中Cr(Ⅲ)回收与再利用工艺如下(硫酸浸液中金属离子主要是Cr3+ , 其次是Fe3+ , Fe2+ , Al3+ , Ca2+ , Mg2+) 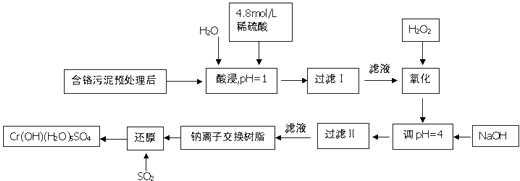
常温下部分阳离子的氢氧化物形成沉淀时溶液的pH见下表:
阳离子 | Fe3+ | Fe2+ | Mg2+ | Al3+ | Ca2+ | Cr3+ |
开始沉淀时的pH | 1.9 | 7.0 | 9.6 | 4.2 | 9.7 | ﹣ |
沉淀完全时的pH | 3.2 | 9.0 | 11.1 | 8.0 | 11.7 | 9.0(>9.0溶解) |
(1)酸浸时,为了提高浸取率可采取的措施是(至少一条)
(2)调pH=4.0是为了除去(填Fe3+ , Al3+ , Ca2+ , Mg2+)
(3)钠离子交换树脂的原理为Mn++n NaR→MRn+nNa+ , 被交换的杂质离子是(填Fe3+ , Al3+ , Ca2+ , Mg2+)
(4)试配平下列氧化还原反应方程式:Na2Cr2O7+SO2+H2O=Cr(OH)(H2O)5SO4+Na2SO4 .
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】椰树牌天然矿泉水的成分:含钠46.31g/L、含钙35.11g/L、含碘0.051g/L…,这里所标成分钠、钙、碘指的是( )
A.元素
B.单质
C.原子
D.氧化物
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列叙述正确的是( )
A.1molCO2 的质量为44g/mol
B.物质的量就是物质的质量
C.气体摩尔体积约为22.4L/mol
D.NA个CO2的质量(以克为单位)与CO2的相对分子质量在数值上相同
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究小组为了验证反应物浓度对反应速率的影响,选用硫酸酸化的高锰酸钾溶液与草酸溶液在室温下进行反应. 实验中所用的草酸为稀溶液,可视为强酸.
(1)将高锰酸钾氧化草酸的离子方程式补充完整. 2MnO4﹣+C2O42﹣+=2 Mn2++CO2↑+H2O
(2)该小组进行了实验I,数据如表.
H2SO4溶液 | KMnO4溶液 | H2C2O4溶液 | 褪色时间(分:秒) |
1mL 2mol/L | 2mL 0.01mol/L | 1mL 0.1mol/L | 2:03 |
1mL 2mol/L | 2mL 0.01mol/L | 1mL 0.2mol/L | 2:16 |
一般来说,其他条件相同时,增大反应物浓度,反应速率.
但分析实验数据,得到的结论是 .
(3)该小组欲探究出现上述异常现象的原因,在实验I的基础上,只改变草酸溶液浓度进行了实验II,获得实验数据并绘制曲线图如图. 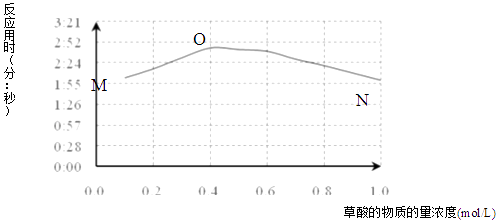
①用文字描述曲线图表达的信息 .
②该小组查阅资料获取如下信息,其中能够解释MO变化趋势的是 .
a | KMnO4与H2C2O4反应是分步进行的,反应过程中生成Mn(VI)、Mn(III)、Mn(IV),最终变为无色的Mn(II).(括号中罗马数字表示锰的化合价) |
b | 草酸根易与不同价态锰离子形成较稳定的配位化合物. |
c | 草酸稳定性较差,加热至185℃可分解. |
(4)该小组为探究ON段曲线变化趋势的原因,又进行了实验III,所得数据如表.
H2SO4溶液 | Na2SO4固体 | KMnO4溶液 | H2C2O4溶液 | 褪色时间(分:秒) |
1mL 0.1mol/L | 1.9×10﹣3mol | 2mL 0.01mol/L | 1mL 0.2mol/L | 16:20 |
1mL 0.5mol/L | 1.5×10﹣3mol | 2mL 0.01mol/L | 1mL 0.2mol/L | 8:25 |
1mL 1.0mol/L | 1.0×10﹣3mol | 2mL 0.01mol/L | 1mL 0.2mol/L | 6:15 |
1mL 2.0mol/L | 0 | 2mL 0.01mol/L | 1mL 0.2mol/L | 2:16 |
该小组进行实验III的目的是 .
(5)综合实验I、II、III,推测造成曲线MN变化趋势的原因.为验证该推测还需要补充实验,请对实验方案进行理论设计.
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是向MgCl2、AlCl3混合溶液中,开始滴加7 mL试剂A,之后改滴加试剂B,所得沉淀物质的量y (mol) 与试剂体积V(mL)间的关系如图所示。(试剂A、B分别是NaOH 溶液盐酸中的一种)
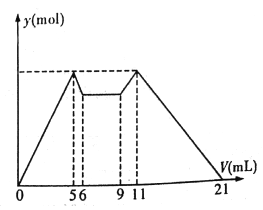
以下结论不正确的是
A. A是NaOH 溶液,B是盐酸
B. 原混合液中,c(Al3+) :c(Mg2+) :c(Cl-)=1:1:5
C. c(NaOH) :c(HCl)=1:2
D. 从6 到9 的过程中,发生的反应的离子反应方程式是H+ +OH-=H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】图为苯和溴的取代反应的实验装置图,其中A为由具有支管的试管制成的反应容器,在其下端开了一个小孔,塞好石棉绒,再加入少量铁屑粉. 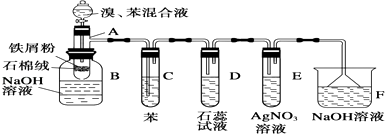
填写下列空白:
(1)向反应容器A中逐滴加入溴和苯的混合液,几秒钟内就发生反应.写出A中所发生反应的化学方程式(有机物写结构简式): .
(2)试管C中苯的作用是 . 反应开始后,观察D和E两试管,看到的现象为 .
(3)反应2~3min后,在B中的NaOH溶液里可观察到的现象是 .
(4)在上述整套装置中,具有防倒吸作用的仪器有(填字母).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮的单质及其化合物性质多样,用途广泛. 完成下列填空.
(1)科学家正在研究利用催化技术将超音速飞机尾气中的NO和CO转变成CO2和N2:2NO+2CO ![]() 2CO2+N2+Q(Q>0) 某温度下测得该反应在不同时间的CO浓度如表:
2CO2+N2+Q(Q>0) 某温度下测得该反应在不同时间的CO浓度如表:
时间(s) | 0 | 1 | 2 | 3 | 4 | 5 |
c(CO) | 3.60×10﹣3 | 3.05×10﹣3 | 2.85×10﹣3 | 2.75×10﹣3 | 2.70×10﹣3 | 2.70×10﹣3 |
该反应平衡常数K的表达式为;温度升高,K值(选填“增大”、“减小”、“不变”);前2s内的平均反应速率v(N2)=;若上述反应在密闭容器中发生,达到平衡时能提高NO转化率的措施之一是 .
(2)工业合成氨的反应温度选择500℃左右的原因是 .
(3)实验室在固定容积的密闭容器中加入1mol氮气和3mol氢气模拟工业合成氨,反应在一定条件下已达到平衡的标志是 . a.N2、H2、NH3的浓度之比为1:3:2
b.容器内的压强保持不变
c.N2、H2、NH3的浓度不再发生变化
d.反应停止,正、逆反应的速率都等于零
(4)常温下向含1mol溶质的稀盐酸中缓缓通入1mol NH3(溶液体积变化忽略不计),反应结束后溶液中离子浓度由大到小的顺序是;在通入NH3的过程中溶液的导电能力(选填“变大”、“变小”、“几乎不变”).
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com