
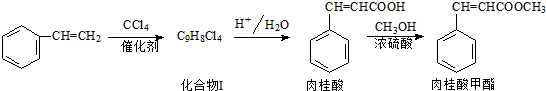
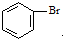
 和CH=CHCOOH反应制得,该反应的反应类型是
和CH=CHCOOH反应制得,该反应的反应类型是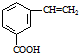 )是肉桂酸的同分异构体,下列有关化合物II和肉桂酸的说法正确的是
)是肉桂酸的同分异构体,下列有关化合物II和肉桂酸的说法正确的是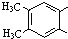 ,它在稀硫酸中能水解,且水解产物经聚合反应后得到高聚物.化合物Ⅲ有多种结构,写出其中一种的结构简式
,它在稀硫酸中能水解,且水解产物经聚合反应后得到高聚物.化合物Ⅲ有多种结构,写出其中一种的结构简式 ;
; 在酸性条件下发生水解生成肉桂酸:
在酸性条件下发生水解生成肉桂酸: ,肉桂酸与甲醇发生酯化反应生成肉桂酸甲酯:
,肉桂酸与甲醇发生酯化反应生成肉桂酸甲酯: ;
; 和CH=CHCOOH与产物
和CH=CHCOOH与产物 的官能团变化判断其反应类型;
的官能团变化判断其反应类型; 分子中含有羧基、碳碳双键,根据
分子中含有羧基、碳碳双键,根据 与肉桂酸的结构简式进行解答;
与肉桂酸的结构简式进行解答; ;
; 在酸性条件下发生水解生成肉桂酸:
在酸性条件下发生水解生成肉桂酸: ,肉桂酸与甲醇发生酯化反应生成肉桂酸甲酯:
,肉桂酸与甲醇发生酯化反应生成肉桂酸甲酯: ,
, ;
; 和CH=CHCOOH反应制得,二者反应生成
和CH=CHCOOH反应制得,二者反应生成 和HBr,该反应为取代反应,
和HBr,该反应为取代反应, ,其分子中含有碳碳双键,可以与强氧化剂发生氧化反应,故A正确;
,其分子中含有碳碳双键,可以与强氧化剂发生氧化反应,故A正确; 中含有官能团羧基,能够与金属钠反应生成氢气,故B错误;
中含有官能团羧基,能够与金属钠反应生成氢气,故B错误; 不含能够发生水解的官能团,如酯基、卤素原子等,所以不能发生水解反应,故C错误;
不含能够发生水解的官能团,如酯基、卤素原子等,所以不能发生水解反应,故C错误;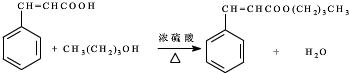 ,
, ;
;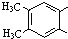 ,它在稀硫酸中能水解,且水解产物经聚合反应后得到高聚物,说明其分子中含有酯基,结合肉桂酸甲酯
,它在稀硫酸中能水解,且水解产物经聚合反应后得到高聚物,说明其分子中含有酯基,结合肉桂酸甲酯 的结构可知,含有
的结构可知,含有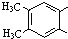 结构其含有酯基,其不饱和度还差1,所以其酯中含有环状条件,如:
结构其含有酯基,其不饱和度还差1,所以其酯中含有环状条件,如: ,故答案为:
,故答案为: .
.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
| A、Cu2+、Na+、SO42-、Cl- |
| B、K+、Na+、HCO3-、NO3- |
| C、OH-、HCO3-、Ca2+、Na+ |
| D、Ba2+、Na+、OH-、NO3- |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、氯气通入碘化钾溶液:Cl2+I-=Cl-+I2 |
| B、稀盐酸与氨水混合:H++OH-=H2O |
| C、碳酸钠溶液与稀盐酸混合:CO32-+2H+=H2O+CO2↑ |
| D、稀硫酸滴在铜片上:Cu+2H+=Cu2++H2↑ |
查看答案和解析>>
科目:高中化学 来源: 题型:
 食醋分为酿造醋和配制醋两种.国家标准规定酿造食醋总酸含量不得低于3.5g/100mL.
食醋分为酿造醋和配制醋两种.国家标准规定酿造食醋总酸含量不得低于3.5g/100mL.查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、此法的优点之一是原料来源丰富 |
| B、①②③步骤的目的是从海水中提取MgCl2 |
| C、以上提取镁的过程中涉及化合、分解和复分解反应 |
| D、第④步电解时阴极产生氯气 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com