

分析 (1)①根据温度对化学平衡的影响结合图象分析该反应是放热反应还是吸热反应;
②根据T1的T2关系结合图象分析平衡的移动,根据反应物和生成物物质的量的改变引起化学平衡常数的改变判断K1、K2的关系;根据图象中曲线及曲线上、下方区域表示的含义分析,曲线表示平衡状态,曲线下方表示向正反应方向进行,曲线上方表示向逆反应方向进行;
(2)①根据能量变化示意图中能量数据的含义来回答;
②由图甲可知,N2和H2反应生成1molNH3放出的热量为(Q2-Q1)kJ,注明物质的聚集状态与反应热书写热化学方程式.
解答 解:(1)①根据图象可知:升高温度,SO3的平衡含量减少,说明升高温度,平衡向逆反应方向移动.根据平衡移动原理:升高温度,平衡向吸热反应方向移动,因此2SO2(g)+O2(g)?2SO3(g)的正反应是放热反应,△H<0;若在恒温、恒压条件下向上述平衡体系中通入氦气,则容器的容积扩大,物质的浓度减小,容器内气体的压强减小,平衡向气体体积增大的方向移动,因此平衡逆向移动.即向左移动,故答案为:<;向左;
②由于升高温度,平衡逆向移动,所以若温度为T1、T2,反应的平衡常数分别为K1,K2,则K1>K2;温度为T1时,反应进行到状态D时,未达到平衡时的SO3的浓度,所以反应正向进行,则v 正>v逆,故答案为:>;>;
(2)图示是一定的温度和压强下N2(g)和H2(g)反应生成lmol NH3(g)过程中能量变化示意图,图中E1 表示的是正反应的活化能(或正反应发生需要的最低能量);E2表示的意义是E2:逆反应的活化能(或逆反应发生需要的最低能量),
故答案为:正反应的活化能;逆反应的活化能;
②根据图示可知每产生1mol NH3(g)放出能量是(Q2-Q1)kJ,因此工业合成氨的热化学方程式是$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=(Q1-Q2)kJ/mol,
故答案为:$\frac{1}{2}$N2(g)+$\frac{3}{2}$H2(g)=NH3(g)△H=(Q1-Q2)kJ/mol.
点评 本题综合考查化学平衡的影响因素,化学平衡的计算与判断,为高考常见题型和高频考点,注意把握图象的分析与判断,本题还要注意反应热与焓变,把握活化能与反应热的关系,难度不大.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案 目标测试系列答案
目标测试系列答案科目:高中化学 来源: 题型:选择题
| A. | Na2O2与Na2O | B. | Na2O2 | C. | Na2O2与Na | D. | Na和Na2O |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 序号 | 实验内容 | 实验现象 | 离子方程式 | 实验结论 |
| ① | 在FeCl2溶液中滴入适量氯水 | 溶液由浅绿色变为黄色 | 2Fe2++Cl2=2Fe3++2Cl- | Fe2+具有还原性 |
| ② | 在FeCl2溶液中加入锌片 | (不写) | Zn+Fe2+=Zn2++Fe | Fe2+具有氧化性 |
| ③ | 在FeCl3溶液中加入足量铁粉 | 溶液由黄色变为浅绿色 | Fe+2Fe3+=3Fe2+ | Fe3+具有氧化性 |
| ④ | 在FeCl3溶液中滴入适量KI溶液和淀粉溶液 | 变蓝色 | 2Fe3++2I-=2Fe2++I2 | Fe3+具有氧化性 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
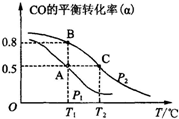 空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.
空气质量与我们的健康息息相关,目前我国通过监测6项污染物的质量浓度来计算空气质量指数(AQI),SO2、NO2和CO是其中3项中的污染物.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
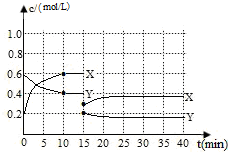 已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物浓度随时间变化关系如下图所示.X与Y两条曲线中,Y表示N2O4浓度随时间的变化
已知NO2和N2O4可以相互转化:2NO2(g)?N2O4(g)△H<0.现将一定量NO2和N2O4的混合气体通入体积为1L的恒温密闭容器中发生上述反应,反应物浓度随时间变化关系如下图所示.X与Y两条曲线中,Y表示N2O4浓度随时间的变化查看答案和解析>>
科目:高中化学 来源: 题型:解答题
时间s 浓度mol/L | 0 | 20 | 40 | 60 | 80 | 100 |
| c(N2O4) | 0.100 | c1 | 0.050 | c3 | a | b |
| c(NO2) | 0.000 | 0.060 | c2 | 0.120 | 0.120 | 0.120 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
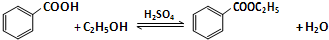
| 物质 | 颜色状态 | 密度/g/cm3 | 熔点/℃ | 沸点/℃ |
| 苯甲酸 | 白色固体 | 1.2659 | 122 | 249 |
| 苯甲酸乙酯 | 无色液体 | 1.05 | -34.6 | 212.6 |
| 乙酸 | 无色液体 | 1.0492 | 16.6 | 117.9 |
| 乙醇 | 无色液体 | 0.789 | -117.3 | 78.5 |
| 乙酸乙酯 | 无色液体 | 0.894-0.898 | -83.6 | 77.1 |
| 乙醚 | 无色液体 | 0.713 | -116.3 | 34.6 |
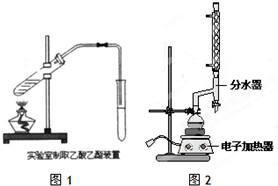
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
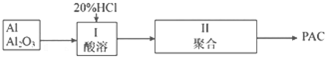
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com