
| A、容器中压强不随时间的变化而改变 |
| B、容器中SO2和SO3的浓度相同 |
| C、容器中SO2、O2、SO3的物质的量为2:1:2 |
| D、容器中SO2、O2、SO3共存 |


科目:高中化学 来源: 题型:
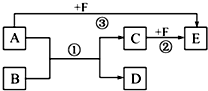 已知:A、B、C、D、E、F是中学化学教材中六种常见的物质,它们之间有如图所示的相互转化关系(反应条件及部分产物未标出).请回答下列问题:
已知:A、B、C、D、E、F是中学化学教材中六种常见的物质,它们之间有如图所示的相互转化关系(反应条件及部分产物未标出).请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:
| A、煤、石油、天然气均为化石能源 |
| B、化石燃料在燃烧过程中能产生污染环境的SO2等有害气体 |
| C、直接燃烧煤不如将煤进行深加工后再燃烧效果好 |
| D、化石能源是可再生能源 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、稀释浓硫酸时,应将浓硫酸沿玻璃棒注入盛有水的烧杯,同时边加边搅拌. |
| B、某溶液加入硝酸酸化的氯化钡溶液产生白色沉淀,则溶液中一定含有SO42-离子 |
| C、制作印刷电路板的过程中常用氯化铁溶液与铜反应 |
| D、某气体通入品红溶液能使品红褪色,则该气体不一定是SO2气体. |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、①③④ | B、③④ |
| C、②③④ | D、③④⑤ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、某溶液中c(H+)=c(OH-)=10-8 mol?L-1,该溶液呈中性 |
| B、溶液中若c(H+)>10-7 mol?L-1,则c(H+)>c(OH-),溶液显酸性 |
| C、c(H+)越大,则pH越大,溶液的酸性越强 |
| D、pH为0的溶液,其中只有H+,无OH- |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、常温常压下,18 g H2O含有的原子数为NA |
| B、1.8 g的NH4+离子中含有的电子数为1.1NA |
| C、0℃,101kPa时,1 mol O2和N2的混合气体的总体积约为22.4 L |
| D、2.4 g金属镁变为镁离子时失去的电子数为0.3NA |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com