
互为同分异构体的物质不可能( )
A.具有相同的相对分子质量
B.具有相同的分子式
C.具有相同的组成元素
D.具有相同的熔、沸点
科目:高中化学 来源: 题型:
下列叙述正确的是( )
A.95℃纯水的pH<7,说明加热可导致水呈酸性
B.pH=3的醋酸溶液,稀释至10倍后pH=4
C.0.2 mol·L-1的盐酸与等体积水混合后pH=1
D.pH=3的醋酸溶液与pH=11的氢氧化钠溶液等体积混合后pH=7
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组物质不属于同系物的是( )
①CH2===CH—COOH和C17H33COOH
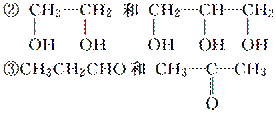
④正丁烷和2,2二甲基丙烷
A.①③ B.①④ C.②③ D.②④
查看答案和解析>>
科目:高中化学 来源: 题型:
某混合烃由两种气态烃组成,取2.24 L该混合烃燃烧后,得到3.36 L CO2和3.6 g水,则下列关于该混合烃的组成判断正确的是(气体体积均在标准状况下测定)( )
A.可能含甲烷
B.一定含乙烷
C.一定是甲烷和乙烯的混合气体
D.可能是甲烷和丙炔的混合气体
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)下表为烯烃类化合物与溴发生加成反应的相对速率(以乙烯为标准):
| 烯烃类化合物 | 相对速率 |
| (CH3)2C===CHCH3 | 10.4 |
| CH3CH===CH2 | 2.03 |
| CH2===CH2 | 1.00 |
| CH2===CHBr | 0.04 |
根据表中数据,总结烯烃类化合物加溴时,反应速率与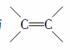 键上取代基的种类、个数间的关系: _______________________________________
键上取代基的种类、个数间的关系: _______________________________________
________________________________________________________________________
________________________________________________________________________
________________________________________________________________________。
(2)下列化合物与氯化氢加成时,取代基对速率的影响与上述规律类似,其中反应速率最慢的是______(填代号)。
A.(CH3)2C===C(CH3)2
B.CH3CH===CHCH3
C.CH2===CH2
D.CH2===CHCl
(3)烯烃与溴化氢、水加成时,产物有主次之分,例如:
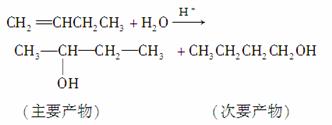
下列框图中B、C、D都是相关反应中的主要产物(部分条件、试剂被略去),且化合物B中仅有4个碳原子、1个溴原子、9个等效氢原子。
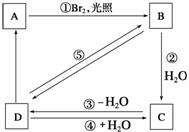
上述框图中,B的结构简式为________________;属于取代反应的有________(填框图中的序号,下同),属于消去反应的有________。
查看答案和解析>>
科目:高中化学 来源: 题型:
下图是一种形状酷似一条小狗的有机物,化学家Tim Rickard将其取名为“doggyene”,下列有关doggycene的说法正确的是( )
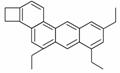
A.“doggycene”中所有碳原子不可能处于同一平面上
B.该物质的分子式为C26H30
C.常温下该有机物为气态
D.1 mol该物质在氧气中完全燃烧生成CO2和H2O的物质的量之比为2∶1
查看答案和解析>>
科目:高中化学 来源: 题型:
A、B、D、E、F为短周期元素,非金属元素A最外层电子数与其周期数相同,B的最外层电子数是其所在周期数的2倍。B在D中充分燃烧能生成其最高价化合物BD2。E+与D2-具有相同的电子数。A在F中燃烧,发出苍白色火焰,产物溶于水得到一种强酸。回答下列问题:
(1)写出一种工业制备单质F的化学方程式:____________________________。
(2)B、D、E组成的一种盐中,E的质量分数为43%,其俗名为___________, 请用离子方程式解释该溶液呈碱性的原因____________________________________________;
(3)实验室用F从含碘废液(除H2O外,含有CCl4、I2、I-等)中回收碘,其实验过程如下:
|
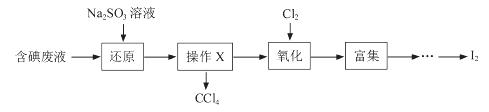
①向含碘废液中加入稍过量的Na2SO3溶液,将废液中的I2还原为I-,其离子方程式为__________ ;
②操作X的名称为___________________。
③已知:5SO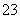 +2IO
+2IO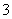 +2H+===I2+5SO
+2H+===I2+5SO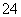 +H2O,某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO
+H2O,某含碘废水(pH约为8)中一定存在I2,可能存在I-、IO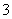 中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO
中的一种或两种。请补充完整检验含碘废水中是否含有I-、IO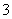 的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验没有碘单质存在;___________________________________;
的实验方案:取适量含碘废水用CCl4多次萃取、分液,直到水层用淀粉溶液检验没有碘单质存在;___________________________________;
另从水层取少量溶液,加入1~2 mL淀粉溶液,加盐酸酸化,滴加Na2SO3溶液,若溶液变蓝,说明废水中含有IO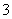 ;若溶液不变蓝,说明废水中不含有IO
;若溶液不变蓝,说明废水中不含有IO 。
。
(实验中可供选择的试剂:稀盐酸、淀粉溶液、FeCl3溶液、Na2SO3溶液。)
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室合成乙酸乙酯的步骤如下:在圆底烧瓶内加入乙醇、浓硫酸和乙酸,瓶口竖直安装通有冷却水的冷凝管(使反应混合物的蒸气冷凝为液体流回到烧瓶内),加热回流一段时间后换成蒸馏装置进行蒸馏,得到含有乙醇、乙酸和水的乙酸乙酯粗产品。请回答下列问题:
(1)在烧瓶中除了加入乙醇、浓硫酸和乙酸外,还应放入________,目的是
________________________________________________________________________。
(2)反应中加入过量的乙醇,目的是
________________________________________________________________________
________________________________________________________________________。
(3)如果将上述实验步骤改为在蒸馏烧瓶内先加入乙醇和浓硫酸,然后通过分液漏斗边滴加醋酸,边加热蒸馏。这样操作可以提高酯的产率,其原因是__________________
________________________________________________________________________。
(4)现拟分离含乙酸、乙醇和水的乙酸乙酯粗产品,下图是分离操作步骤流程图。请在图中圆括号内填入适当的试剂,在方括号内填入适当的分离方法。

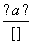
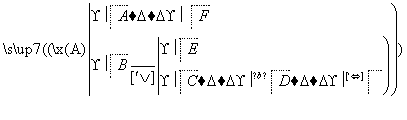
试剂a是____________,试剂b是________;分离方法①是________,分离方法②是________,分离方法③是________________。
(5)在得到的A中加入无水碳酸钠粉末,振荡,目的是____________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com