
按要求写出下列反应的方程式
⑴工业用石英制取粗硅的反应方程式:_______________________________;
⑵工业用赤铁矿做原料炼铁的反应方程式: ;
⑶金属铝与NaOH溶液反应的离子方程式:_______________________________;
⑷FeSO4溶液中滴加双氧水的离子方程式: ;
⑸酸性条件下, MnO4—被SO2还原为Mn2+的离子方程式:___________________________;
 中考解读考点精练系列答案
中考解读考点精练系列答案科目:高中化学 来源: 题型:
某同学按下述操作配制500 mL 0.2 mol·L-1Na2SO4溶液,请回答有关问题。
| 实验步骤 | 有关问题 |
| ①计算所需Na2SO4的质量 | 需要称量Na2SO4的质量为________g |
| ②称量Na2SO4固体 | 称量需要用到的主要仪器是:________________ |
| ③将Na2SO4加入100 mL烧杯中,并加入适量水 | 为了加快溶解速率,可以采取哪些措施?________________________________________________________________________ |
| ④将烧杯中溶液转移至500 mL容量瓶中 | 为了防止溶液溅出,应采取什么措施?________________________________________________________________________ |
| ⑤向容量瓶中加蒸馏水至刻度线 | 在进行此操作时当加水至刻度线1~2 cm处应如何操作?________________________________________________________________________ |
(1)上述实验中使用容量瓶前应_______________________________。
(2)取出该Na2SO4溶液10 mL加水稀释到100 mL,稀释后溶液中Na+的物质的量浓度是________。
(3)若进行⑤步操作时加蒸馏水超过刻度线,则需________。
(4)在实验中,以下操作对实验结果没有影响的是________。
A.没有将洗涤液转移到容量瓶中
B.定容时仰视刻度线
C.转移前没有将使用的容量瓶烘干
D.定容摇匀后,发现凹液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于物质的量浓度表述正确的是( )
A.0.3 mol·L-1的Na2SO4溶液中含有Na+和S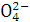 的总物质的量为0.9 mol·L-1
的总物质的量为0.9 mol·L-1
B.当1 L水吸收22.4 L氨气时所得氨水的浓度不是1 mol·L-1,只有当22.4 L(标准状况)氨气溶于水制得1 L氨水时,其浓度才是1 mol·L-1
C.在K2SO4和NaCl的中性混合水溶液中,如果Na+和S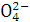 的物质的量相等,则K+和Cl-的物质的量浓度一定相同
的物质的量相等,则K+和Cl-的物质的量浓度一定相同
D.10℃时,100 mL 0.35 mol·L-1的KCl饱和溶液蒸发掉5 g水,冷却到10℃时,其体积小于100 mL,它的物质的量浓度仍为0.35 mol·L-1
查看答案和解析>>
科目:高中化学 来源: 题型:
20世纪,化学科学经历了迅速发展的百年,取得了若干项重大成就。下列各项中,不属于这个时期的重大化学成就的是( )
A.放射性元素的发现 B.现代量子化学理论的建立
C.蛋白质的人工合成 D.制陶技术的成熟应用
查看答案和解析>>
科目:高中化学 来源: 题型:
(1)“绿色化学”是21世纪化学发展的主导方向。“绿色化学”要求从根本上消除污染,是一门能彻底阻止污染产生的科学。它包括“绿色生产”和“绿色销毁”等内容。据报道,某地在整顿音像市场的活动中,查获了一大批盗版光盘,并进行了“绿色销毁”。以下做法中,属于“绿色销毁”的是________(填字母)。
A.泼上汽油焚烧 B.倾倒入江河中
C.深埋于土壤中 D.碾压粉碎后再回收利用
(2)化学是一门具有创造性的科学,它的特征是_____________________。同时,它也是一门实用性科学,在人类生产和生活中起着重要的作用。
查看答案和解析>>
科目:高中化学 来源: 题型:
已知下列元素的原子半径:
| 原子 | N | S | O | Si |
| 半径r/10-10 m | 0.75 | 1.02 | 0.73 | 1.11 |
根据以上数据判断,磷原子的半径可能是( )
A.1.10×10-10 m B.0.80×10-10 m
C.0.70×10-10 m D.1.20×10-10 m
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com