
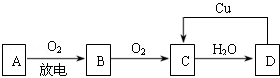
���� CΪ����ɫ���壬��C��NO2��NO2����ˮ���������NO��A�ǿ����е���Ҫ�ɷ֣����ܺ�������Ӧ������A�ǵ�������B��NO��D����Cu��Ӧ�õ�NO2����DΪHNO3���ݴ˽��
��� �⣺CΪ����ɫ���壬��C��NO2��NO2����ˮ���������NO��A�ǿ����е���Ҫ�ɷ֣����ܺ�������Ӧ������A�ǵ�������B��NO��D����Cu��Ӧ�õ�NO2����DΪHNO3��
��1��������������֪��AΪN2��CΪNO2��
�ʴ�Ϊ��N2��NO2��
��2��ͼʾD��C�Ĺ����з�����Ӧ�Ļ�ѧ����ʽ��Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O����Ӧ��HNO3����NԪ�ػ��ϼ۽��ͣ�������ֳ�ǿ�����ԣ�
�ʴ�Ϊ�������ԣ�
��3��C��NO2��DΪHNO3��C��D��Ӧ�Ļ�ѧ����ʽΪ3NO2+H2O=NO+2HNO3��
�ʴ�Ϊ��3NO2+H2O=NO+2HNO3��
��4��D��C�����з�����Ӧ�Ļ�ѧ����ʽ��Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��
�ʴ�Ϊ��Cu+4HNO3��Ũ��=Cu��NO3��2+2NO2��+2H2O��
���� ����������ͼ�⣬�漰���鵪���仯������й�ת�������ͼ��ķ�������ؼ�����Ѱ�ҡ�ͻ�ƿڡ�����ͻ�ƿڡ�����ץ���ء��֣�����������ɫ������״̬��������ζ�����ⷴӦ���������������Ʒ���������;�ȣ��Ƚϻ�����



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2��1 | B�� | l��2 | C�� | l��1 | D�� | 3��l |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
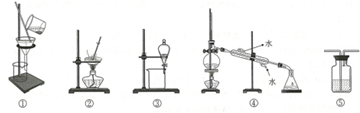
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �÷�Ӧ��ϵ��Au2O�������� | |
| B�� | Na2S4O6�ǻ�ԭ���� | |
| C�� | �÷�Ӧ��ϵ����ԭ���õ�Ԫ����Au2O��+1�۵�Au | |
| D�� | �÷�Ӧ��ϵ��ÿת��2mol����������1molH2O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
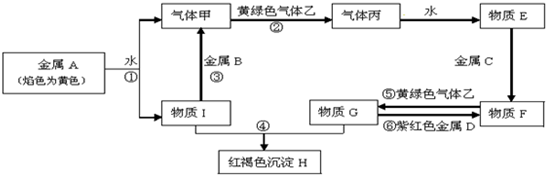
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 2.4gþԭ�ӱ������ʱ��ʧȥ�ĵ�����Ϊ0.3NA | |
| B�� | 22.4L���飨CH4��������ԭ����Ϊ5NA | |
| C�� | 98 g H2SO4��98 g H3PO4��������ԭ��������4NA | |
| D�� | ���ʵ���Ũ��Ϊ0.5 mol/L��MgCl2��Һ�У�����Cl- ����Ϊ NA |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | BaCl2 | B�� | NaOH | C�� | Ba��NO3��2 | D�� | Ba��OH��2 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | SO2����Ư���ԣ���ʹƷ����Һ������KMnO4��Һ��ɫ�ҳ���ʳƷ��Ư�� | |
| B�� | ����̿��H2O2��O3�ȶ���Ư���� | |
| C�� | �������������ˮ����Ư���� | |
| D�� | Na2O2Ҳ��Ư���ԣ���Ư��ԭ����SO2���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com