
| A. | 原溶液一定存在NH4+、I- | |
| B. | 原溶液一定不含Ba2+、Fe3+、I- | |
| C. | 原溶液可能存在K+、Fe3+、SO42- | |
| D. | 另取试液滴加足量盐酸、BaCl2溶液,即可确定溶液所有的离子组成 |
分析 某溶液可能含有NH4+、K+、Ba2+、Fe3+、I-、SO32-、SO42-中的几种,现取100mL溶液加入氯水,溶液呈无色,还原性SO32->I-,溶液中不含I-,但溶液中一定含SO32-,由于有SO32-则无Ba2+;继续滴加足量HNO3和Ba(NO3)2混合溶液,产生沉淀,此沉淀为BaSO4,沉淀经洗涤、高温干燥后质量为4.66g,即BaSO4的物质的量为0.02mol,但由于溶液中一定含SO32-,故生成的0.02molBaSO4中的SO42-可能全部来自于被氧化的SO32-,也可能溶液中原来含有SO42-;滤液加足量NaOH溶液、加热,生成气体为NH3,即原来溶液中一定含NH4+,在标准状况下体积为1120mL,故NH4+的物质的量为0.05mol,根据溶液的电中性来判断K+的存在.
解答 解:现取100mL溶液加入少量氯水,溶液呈无色,由于还原性SO32->I-,故溶液中不含I-,故溶液中一定含SO32-,由于Ba2+与SO32-不能共存,故溶液中无Ba2+;继续滴加足量HNO3和Ba(NO3)2混合溶液,产生沉淀,此沉淀为BaSO4,沉淀经洗涤、高温干燥后质量为4.66g,即BaSO4的物质的量为0.02mol,即SO42-的物质的量为0.02mol,但由于溶液中一定含SO32-,故生成沉淀中的0.02molSO42-可能全部来自于被氧化的SO32-,也可能部分是溶液中原来含有SO42-,但SO32-和SO42-的物质的量之和必须为0.02mol;滤液加足量NaOH溶液、加热,生成气体为NH3,即原来溶液中一定含NH4+,在标准状况下体积为1.12L,故NH4+的物质的量为0.05mol.由于0.02molSO32-(或SO32-和SO42-)带0.04mol负电荷,而0.05molNH4+带0.05mol正电荷,而溶液要保持电中性,故溶液中一定含I-,一定不含铁离子,可能含K+.即溶液中一定含NH4+、SO32-、I-;一定不含:Ba2+、Fe3+;可能含SO42-、K+,另取试液滴加足量盐酸、BaCl2溶液,只能检验出溶液中含不含SO42-,对K+的存在不能确定,
故选B.
点评 本题考查了溶液中离子的检验和确定,应注意根据溶液的电中性来确定I-的存在,难度较大.


 开心快乐假期作业暑假作业西安出版社系列答案
开心快乐假期作业暑假作业西安出版社系列答案科目:高中化学 来源: 题型:选择题
| A. | 1mol A 从酸中置换H+生成的H2比1 mol B从酸中置换H+生成的H2多 | |
| B. | 常温时,A能从水中置换出氢,而B不能 | |
| C. | A原子的最外层电子数比B原子的最外层电子数少 | |
| D. | A原子电子层数比B原子的电子层数多 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
| 实验步骤 | 现象 | 结论 |
| 取少量NaOH溶液样品于试管中,先滴加足量的CaCl2溶液,然后再滴加酚酞试液. | NaOH溶液部分变质 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
| 要提纯的物质(杂质) | C2H5OH (H2O) | CH3CH2OH (CH3COOH) | C6H5Br (Br2) | C6H6 (C6H5OH) |
| 选用试剂(1) | c | b或d | b | b |
| 分离方法(2) | C | C | B | B |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1s22s22p63s23p64s1 | B. | 1s22s22p63s23p63d104s1 | ||
| C. | 1s22s22p63s23p63d104s24p5 | D. | 1s22s22p63s23p63d54s2 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 0.5L 0.1mol/L的NaCl溶液 | B. | 1L 0.2mol/L的MgCl2溶液 | ||
| C. | 1L 0.3mol/L盐酸溶液 | D. | 100mL 0.2mol/L的AlCl3溶液 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
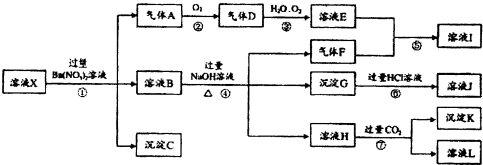
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 以煤、石油和天然气为主要原料生产的合成材料是塑料、合成橡胶、合成纤维 | |
| B. | 煤是工业上获得芳香烃的一种重要来源 | |
| C. | 石油的裂解是为了提高轻质油(例如汽油)的产量 | |
| D. | 天然气的主要成分是甲烷,属于不可再生资源 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com