
| A. | 硫酸与氢氧化钡反应:SO42-+Ba2+═BaSO4↓ | |
| B. | 硫酸镁溶液跟氢氧化钡溶液反应:SO42-+Ba2+═BaSO4↓ | |
| C. | 醋酸滴在锌片上:Zn+2H+═Zn2++H2↑ | |
| D. | Na2C03溶液与稀H2SO4反应:CO32-+2H+═H2O+CO2↑ |
分析 A.漏掉了生成水的反应;
B.漏掉了生成氢氧化镁沉淀的反应;
C.醋酸为弱酸,离子方程式中醋酸需要保留化学式;
D.碳酸钠与稀硫酸反应生成硫酸钠、二氧化碳气体和水.
解答 解:A.硫酸与氢氧化钡溶液反应生成硫酸钡沉淀和水,正确的离子方程式为:2H++SO42-+Ba2++2OH-=BaSO4↓+2H2O,故A错误;
B.硫酸镁与氢氧化钡溶液反应生成硫酸钡沉淀和氢氧化镁,正确的离子方程式为:SO42-+Ba2++Mg2++2OH-=Mg(OH)2↓+BaSO4↓,故B错误;
C.醋酸需要保留分子式,正确的离子方程式为:Zn+2CH3COOH═Zn2++H2↑+CH3COO-,故C错误;
D.Na2C03溶液与稀H2SO4反应的离子方程式为:CO32-+2H+═H2O+CO2↑,故D正确;
故选D.
点评 本题考查了离子方程式的正误判断,为高考的高频题,属于中等难度的试题,注意掌握离子方程式的书写原则,明确离子方程式正误判断常用方法,如:检查反应物、生成物是否正确,检查各物质拆分是否正确,如难溶物、弱电解质等需要保留化学式,检查是否符合原化学方程式等.


 口算题天天练系列答案
口算题天天练系列答案科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | PH=1的溶液中:Na+Mg2+CH3COO-SO42- | |
| B. | PH=13的溶液中:Ba2+K+Cl-HCO3- | |
| C. | 无色溶液中:K+Fe3+CO32-NO3- | |
| D. | 透明溶液中:Na+NH4+NO3-MnO4- |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①和②一样多 | B. | ②比①多 | C. | ①比②多 | D. | 无法比较 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
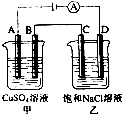 如图两个电解槽中,A、B、C、D均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中不正确的是( )
如图两个电解槽中,A、B、C、D均为石墨电极.若电解过程中共有0.02mol电子通过,下列叙述中不正确的是( )| A. | 甲烧杯中B极上最多可析出铜0.64g | |
| B. | 甲烧杯中A极上电极反应式4OH--4 e-═2H2O+O2↑ | |
| C. | 烧杯中D极上电极反应式为4H++4 e-═2H2↑ | |
| D. | 乙烧杯中滴入酚酞试液,C极附近先变红 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | CO2气体通入石灰水中:CO2+Ca(OH)2═CaCO3↓+H2O | |
| B. | 钠被氧气氧化:4Na+O2═2Na2O | |
| C. | CO气体通过灼热的CuO:CO+CuO$\frac{\underline{\;\;△\;\;}}{\;}$Cu+CO2 | |
| D. | NH3通入硝酸溶液中:NH3+HNO3═NH4NO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com