
已知某温度下CH3COOH和NH3·H2O的电离常数相等,现向10 mL浓度为0.1 mol·L-1的CH3COOH溶液中滴加相同浓度的氨水,在滴加过程中 ( )。
A.水的电离程度始终增大
B.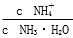 先增大再减小
先增大再减小
C.c(CH3COOH)与c(CH3COO-)之和始终保持不变
D.当加入氨水的体积为10 mL时,c(NH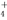 )=c(CH3COO-)
)=c(CH3COO-)
科目:高中化学 来源:2016-2017学年湖北省宜昌市高一上期中化学卷(解析版) 题型:选择题
离子检验的常用方法有三种:
检验方法 | 沉淀法 | 显色法 | 气体法 |
判断的依据 | 反应中有沉淀产生或溶解 | 反应中有颜色变化 | 反应中有气体产生 |
下列离子检验的方法中不合理的是( )
A.CO32-—气体法 B.SO42-—沉淀 法 C.H+—显色法 D.Cl-—气体法
法 C.H+—显色法 D.Cl-—气体法
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一上学期期中化学试卷(解析版) 题型:实验题
大苏打
【有效成分】Na2S2O3
【规格】l000mL
【质量分数】25%
【密度】1.58g·cm-3
(1)某同学取100 mL该试剂,稀释后使用,稀释后的溶液中c(Na+)=________mol·L-1。
(2)该同学参阅该试剂的配方,欲用Na2S2O3固体配制80 mL与所示试剂物质的量浓度相同的溶液,需要称量Na2S2O3固体的质量为 g;所用到的玻璃仪器有玻璃棒、烧杯、量筒和 。
(3)稀硫酸是重要的化工试剂,某实验小组人员用98%(密度为1.84g·cm-3)的浓硫酸配制2000mL2.3mol·L-1的稀硫酸用于实验。
①所配制的稀硫酸中,H+的物质的量浓度为______mol·L-I。
②需用浓硫酸的体积为 mL。
(4)配置一定物质的量浓度的稀硫酸时,下列操作会使所配溶液物质的量浓度偏低的是
A.定容时俯视容量瓶刻度线 |
B.用量筒量取浓硫酸时俯视刻度线 |
C.容量瓶用蒸馏水洗涤干净后没有干燥就移入所配置溶液 |
D.定容后把容量瓶倒置摇匀,发现液面低于刻度线又加水至刻度线。 |
E.加水时超过刻度线,用胶头滴管吸出
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省南阳市高一上学期期中化学试卷(解析版) 题型:选择题
下列说法正确的是( )
A.铜与氯气反应时,剧烈燃烧并产生蓝色的烟
B.次氯酸不如次氯酸盐稳定,故通常用次氯酸盐作为漂白剂和消毒剂的主要成分
C.生活中常用的“84”消毒液中的有效成分是NaCl
D.将金属钠投入硫酸铜溶液中可观察到的实验现象有气体生成,有红色的铜生成
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上调研三化学卷(解析版) 题型:选择题
有①Na2CO3溶液、②CH3COONa溶液、③NaOH溶液各25 mL,物质的量浓度均为0.1 mol·L-1,下列说法正确的是( )。
A.三种溶液pH的大小顺序是③>②>①
B.若将三种溶液稀释相同倍数,pH变化最大的是②
C.若 分别加入25 mL 0.1 mol·L-1盐酸后,pH最大的是①
分别加入25 mL 0.1 mol·L-1盐酸后,pH最大的是①
D.若三种溶液的pH均为9,则物质的量浓度的大小顺序③>①>②
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上调研三化学卷(解析版) 题型:选择题
pH=13的强碱溶液与pH=2的强酸溶液混合,所得溶液的pH=11,则强 碱与强酸的体积比是( ).
碱与强酸的体积比是( ).
A.11∶1 B.9∶1 C.1∶11 D.1∶9
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河北省高二上调研三化学卷(解析版) 题型:选择题
下列事实能说明HNO2为弱电解质的是( )
①0.1 mol/L HNO2溶液的pH=2.1
②常温下NaNO2溶液的pH>7
③用HNO2溶液做导电实验时,灯泡很暗
④HNO2溶液和KCl溶液不发生反应
⑤HNO2能与碳酸钠反应制CO2
⑥HNO2不稳定,易分解
A.①②③ B.①②④⑤ C.①②⑥ D.①②
查看答案和解析>>
科目:高中化学 来源:2017届广东省广州市高三12月模拟化学试卷(解析版) 题型:实验题
Na2S2O3是重要的化工原料,易溶于水,在中性或碱性环境中稳定,在酸性环境下易分解生成S和SO2。某小组设计了如下实验装置制备Na2S2O3(夹持及加热仪器略),总反应为2Na2S+Na2CO3+4SO2  3Na2S2O3+CO2。回答下列问题:
3Na2S2O3+CO2。回答下列问题:
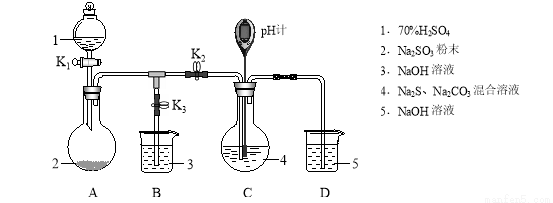
(1)装置A的作用是制备______________,反应的化学方程式为______________。
(2)完成下表实验过程:
操作步骤 | 装置C的实验现象 | 解释原因 |
检查装置气密性后,添加药品 | pH计读数约为13 | 用离子方程式表示(以S2-为例): ① |
打开K2,关闭K3,调节K1使硫酸缓慢匀速滴下 | ⅰ.导管口有气泡冒出, ② ⅱ.pH计读数逐渐 ③ | 反应分步进行: Na2CO3+SO2 2Na2S+3SO2 Na2SO3+S |
当pH计读数接近7时,立即停止通SO2,操作是 ④ | 必须立即停止通SO2的原因是: ⑤ |
(3)Na2S2O3有还原性,可作脱氯剂。向Na2S2O3溶液中通入少量Cl2,某同学预测S2O32-转变为SO42-,设计实验验证该预测:取少量反应后的溶液于试管中,______________。
查看答案和解析>>
科目:高中化学 来源:2017届四川省高三12月月考化学试卷(解析版) 题型:选择题
25℃时,向25 mL 0.1 mol·L-1 NaOH溶液中逐滴加入0.2 mol·L-1醋酸溶液,滴定曲线如图所示,下列说法正确的是
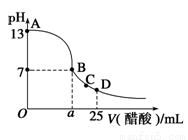
A.在A、B间任一点的溶液中一定都有:c(Na+)>c(CH3COO-)>c(OH-)>c(H+)
B.Ka(CH3COOH)=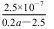
C.C点对应的溶液中,水电离出的H+浓度大于10-7 mol·L-1
D.D点对应的溶液中,存在如下关系:c(CH3COO-)-c(CH3COOH)=2c(H+)-c(OH-)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com