
【题目】2015年巴黎气候变化大会的主题之一是节能减排,开发新能源以及提高能源的利用率再次受到国际社会的高度关注。
(1)近年我国努力调整能源结构,开发新能源。下列物质中,属于可再生能源的是____(填字母)。
A、氢能 B、天然气 C、石油
(2)工业制氢有多种渠道:
①其中一个重要反应是:CO(g) + H2O(g)=CO2(g) + H2(g) ΔH。
已知: C(s,石墨) + O2(g)=CO2(g) ΔH1=-394 kJ/mol
2C(s,石墨) + O2(g)=2CO(g) ΔH2=-222 kJ/mol
H2(g)+ ![]() O2(g)=H2O(g) ΔH3=-242 kJ/mol
O2(g)=H2O(g) ΔH3=-242 kJ/mol
则ΔH=_____kJ/mol。
②一种“金属(M)氧化物循环制氢”的原理如图所示。写出该流程制氢的总反应式:____。

③氢气可用于制备H2O2。已知:H2(g)+A(l)=B(l) ΔH1、O2(g)+B(l)=A(l)+H2O2(l) ΔH2,这两个反应均为自发反应,则H2(g)+O2(g)=H2O2(l)的ΔH____0(填“>”、“<”或“=”)。
(3)工业上可通过CO(g)和H2(g)化合来制备可再生能源CH3OH(g):CO(g)+2H2(g)=CH3OH(g) △H=-99 kJ·mol-l,又知该反应中某些物质分子里的化学键的键能数据如下表:

如CO中的C与O之间为叁键连接,则C≡O键的键能为___________kJ·mol-l。
【答案】A -41 2H2O![]() 2H2↑+O2↑ < 1076
2H2↑+O2↑ < 1076
【解析】
(1)天然气和石油都属于化石燃料,是不可再生能源,属于可再生能源的是氢能,答案为A。
(2)① C(s,石墨) + O2(g)=CO2(g) ΔH1=-394 kJ/mol a
2C(s,石墨) + O2(g)=2CO(g) ΔH2=-222 kJ/mol b
H2(g)+ ![]() O2(g)=H2O(g) ΔH3=-242 kJ/mol c
O2(g)=H2O(g) ΔH3=-242 kJ/mol c
根据盖斯定律将a-![]() b-c得:CO(g) + H2O(g)=CO2(g) + H2(g)的ΔH=-41kJ/mol。
b-c得:CO(g) + H2O(g)=CO2(g) + H2(g)的ΔH=-41kJ/mol。
②一种“金属(M)氧化物循环制氢”的原理如图所示。由流程可以看出,H2O分解生成H2和O2,其中M为催化剂,MxOy为催化剂的中间产物,该流程制氢的总反应式:2H2O![]() 2H2↑+O2↑;
2H2↑+O2↑;
③已知:H2(g)+A(l)=B(l) ΔH1、O2(g)+B(l)=A(l)+H2O2(l) ΔH2,这两个反应均为自发反应,由于均是熵减的反应,则ΔH1<0,ΔH2<0。H2(g)+O2(g)=H2O2(l)的ΔH=ΔH1+ΔH2<0。
(3)依据反应热等于断键吸收的总能量和形成化学键所放出的能量的差值可知C≡O键的键能为:(413×3+343+465-2×436-99)kJ·mol-l=1076kJ·mol-l。


科目:高中化学 来源: 题型:
【题目】下列有关化学反应速率和限度的说法中,不正确的是( )
A. 已知工业合成氨的正反应方向放热,所以升温正反应速率降低,逆反应速率升高
B. 实验室用H2O2分解制备O2,加入MnO2后,反应速率明显加快
C. 2SO2+O2![]() 2SO3反应中,SO2的转化率不能达到100%
2SO3反应中,SO2的转化率不能达到100%
D. 实验室用碳酸钙和盐酸反应制取CO2,用碳酸钙粉末比块状反应要快
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作不能达到实验目的的是( )
A. 用加热的方法除去碳酸钠固体中的碳酸氢钠
B. 加热蒸干溶液,可以得到CuCl2晶体
C. 放在流动的蒸馏水中可除去半透膜中蛋白质溶液里混有的(NH4)2SO4
D. 鉴别NaBr和KI溶液,可分别加新制氯水后,用CCl4萃取
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】(1)如图为干冰的晶体结构示意图。
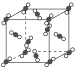
通过观察分析,每个CO2分子周围紧邻等距离的CO2分子有__个。将CO2分子视作质点,设晶胞边长为apm,则紧邻的两个CO2分子的距离为__pm。
(2)在冰晶体中,水分子之间的主要作用力是__,还有__,由于该主要作用力与共价键一样具有__性,故1个水分子周围只有__个紧邻的水分子,这些水分子位于__的顶点。这种排列方式使冰晶体中水分子的空间利用率__(填“较高”或“较低”),故冰的密度比水的密度要__(填“大”或“小”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求书写化学方程式。
(1)乙醇催化氧化____________。
(2)1,2—二溴乙烷与氢氧化钠的醇溶液共热____________。
(3)向苯酚钠溶液中通入少量的CO2_____________。
(4)乙二醛与新制的银氨溶液反应______________。
(5)已知乳酸的结构简式为CH3CH(OH)COOH,写出以乳酸为单体形成的高分子化合物的化学方程式___________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化亚铜(CuCl)是白色粉末,微溶于水,酸性条件下不稳定,易生成金属 Cu 和Cu2+,广泛应用于化工和印染等行业。某研究性学习小组拟热分解 CuC122H2O 制备 CuCl,并进行相关探究。下列说法不正确的是( )

A.途径 1 中产生的Cl2 可以回收循环利用
B.途径 2 中 200℃时反应的化学方程式为:Cu2(OH)2Cl2![]() 2CuO+2HCl↑
2CuO+2HCl↑
C.X 气体是HCl,目的是抑制 CuCl22H2O 加热过程可能的水解
D.CuCl 与稀硫酸反应的离子方程式为:2CuCl+4H++SO42—=2Cu2++2Cl—+SO2↑+2H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作或装置符合实验要求的是()
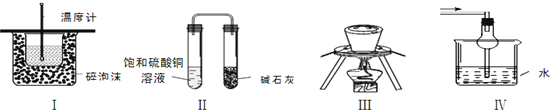
A.装置Ⅰ可用于测定中和热
B.装置Ⅱ装置放置一段时间后,饱和![]() 溶液中不出现蓝色晶体
溶液中不出现蓝色晶体
C.装置Ⅲ中的石英坩埚可用于熔化氢氧化钠
D.装置Ⅳ可用于吸收易溶于水的尾气
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某温度时,在2L密闭容器中X、Y、Z三种气态物质的物质的量(n)随时间(t)变化的曲线如图所示,由图中数据

(1)该反应的化学方程式为______________。
(2)反应开始至2min,用Z表示的平均反应速率为_________。
(3)下列叙述能说明上述反应达到化学平衡状态的是________(填序号)
A.混合气体的总物质的量不随时间的变化而变化
B.混合气体的压强不随时间的变化而变化
C.单位时间内每消耗![]() X,同时生成
X,同时生成![]() Z
Z
D.混合气体的总质量不随时间的变化而变化
E.混合气体的密度不再发生改变
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在给定条件下,下列选项所示的物质间转化均能实现的是( )
A. SO2![]() CaSO3
CaSO3![]() CaSO4
CaSO4
B. Fe![]() Fe2O3
Fe2O3![]() FeCl3
FeCl3
C. HCl(aq) ![]() Cl2
Cl2![]() Ca(ClO)2
Ca(ClO)2
D. Cu2(OH)2CO3![]() CuO
CuO![]() CuCl2(aq)
CuCl2(aq)
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com