
【题目】最活泼的金属元素、最活泼的非金属元素、常温下呈液态的金属(价电子排布为5d106s2)元素分别位于下面元素周期表中的( )

A. s区、p区、ds区 B. s区、p区、d区
C. f区、p区、ds区 D. s区、f区、ds区
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
【题目】下列关于有机物结构、性质的说法正确的是
A. 石油的分馏、裂化和煤的干馏都是化学变化
B. 甲烷的一氯代物只有一种可证明甲烷分子呈正四面体形
C. 邻二甲苯只有一种结构,能证明苯环中不存在碳碳单键和碳碳双键交替的结构
D. 正丁烷和异丁烷的熔沸点相同,它们的一氯取代物都只有两种
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,1mol·L-l的某二元酸H2A溶液中,存在的HA-、A2-的物质的量分数随pH变化的关系如图所示,
下列说法不正确的是
A. H2A的电离方程式为:H2A==H++HA- HA-![]() A2-+H+
A2-+H+
B. 室温下,电离平衡HA-![]() A2-+H+的平衡常数Ka=10-3。
A2-+H+的平衡常数Ka=10-3。
C. 等物质的量浓度NaHA和Na2A溶液等体积混合,离子浓度大小关系为:c(Na+)>c(HA-)>c(A2-)
D. 在Na2A溶液中存在c(Na+)=2c(A2-)+2c(HA-)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】向湿法炼锌的电解液中同时加入Cu和CuSO4,可生成CuCl沉淀除去Cl—,降低对电解的影响,反应原理如下:
Cu(s)+Cu2+(aq)![]() 2Cu+(aq) ΔH1=a kJ·mol-1
2Cu+(aq) ΔH1=a kJ·mol-1
Cl—(aq)+Cu+(aq)![]() CuCl(s) ΔH2=b kJ·mol-1
CuCl(s) ΔH2=b kJ·mol-1
实验测得电解液pH对溶液中残留c(Cl—)的影响如图所示。下列说法正确的是

A. 溶液pH越大,Ksp(CuCl)增大
B. 向电解液中加入稀硫酸,有利于Cl-的去除
C. 反应达到平衡增大c(Cu2+),c(Cl—)减小
D. ![]() Cu(s)+
Cu(s)+![]() Cu2+(aq)+Cl—(aq)
Cu2+(aq)+Cl—(aq)![]() CuCl(s)的ΔH=(a+2b) kJ·mol-1
CuCl(s)的ΔH=(a+2b) kJ·mol-1
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是钢铁电化学保护的示意图。分析正确的是

A. 若a、b两端用导线相连,Fe作正极
B. 若a、b两端用导线相连,Zn被还原
C. 若a、b两端与电源相连,Fe作阳极
D. 若a、b两端与电源相连,Zn极得电子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】硫及其化合物在工业生产、生活中有重要的用途。
(1)硫原子最外层电子轨道表示式为__________。与电子排布式相比,轨道表示式还描述了核外电子运动状态中的______和______。
(2)S、Cl、N三种元素常见的氢化物中,写出属于非电解质的电子式___________。已知PbS与O2在高温时生成铅的氧化物和SO2,化学平衡常数(K)的表达式为:K=![]() 。
。
(3)写出上述反应的化学方程式__________________________。在2L高温密闭容器中加入PbS固体和O2,0~5min内气体质量增加1.6g,则5min内SO2的平均反应速率___________________。
(4)上述反应达到平衡后,说法正确的是_________(选填编号)。
a. 速率关系:2v(O2)=3v(SO2)
b. 气体密度随着PbS的质量增加而增大
c. 每生成1.5molO2,同时消耗1molSO2
d. 压缩体积到新平衡,浓度增大的倍数:O2>SO2

(5)向NaOH溶液中缓慢通入SO2至过量,反应过程中某微粒X的物质的量浓度随通入SO2的体积变化如图所示。该微粒X为_________。SO2过量时溶液中仍存在微粒X,解释原因。______________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】E是一种能发生加聚反应的有机合成中间体,合成E的路线如下。

(1)反应①的类型是________________;反应②的试剂和条件是__________________。
(2)写出反应③的化学方程式_______________________________。
(3)D的结构简式___________。
D有多种同分异构体,写出一种符合下列要求的结构简式____________。
i. 含有苯环 ii. 能发生水解反应 iii. 苯环上的一溴代物有两种
(4)通过反应⑤得到E的产率不高,原因是___________________________。
(5)设计一条由CH3CH=CHCH3为原料制备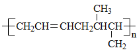 的合成路线。___________
的合成路线。___________
(合成路线常用的表示方法为:X![]() Y……
Y……![]() 目标产物)
目标产物)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,向 20mL0.2mol·L1H2A 溶液中滴加 0.2mol·L1NaOH 溶液,滴加过程中有关微粒的物质的量变化绘制在下图中。下列说法正确的是

A. 当 V(NaOH)=10mL 时,溶液中粒子浓度大小关系为:c(Na+)>c(H2A)>c(HA)>c(H+)>c(OH)
B. 当 V(NaOH)=20 mL 时,溶液中粒子浓度大小关系为:c(Na+)>c(H+)>c(HA)>c(A2)>c(H2A)
C. 当 V(NaOH)=30 mL 时,溶液中存在以下关系:c(A2)+2c(OH)=c(HA)+c(H+)+3c(H2A)
D. 当 V(NaOH)=40mL 时,溶液中存在以下关系:c(Na+)=2[c(A2)+c(HA)+ c(H2A)]
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将0.4molMnO2和100mL12mol/L盐酸混合后加热,反应完全后向留下的溶液中加入足量AgNO3溶液,生成AgCl沉淀物质的量为(不考虑盐酸挥发)
A.等于0.6molB.小于0.6molC.大于0.6molD.等于0.3mol
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com