
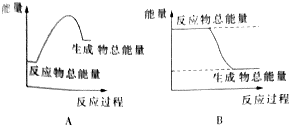
分析 (1)旧键断裂要吸收能量,新键生成要释放能量,当旧键断裂吸收的能量大于新键生成释放的能量时,反应为吸热反应,反之则为放热反应;
(2)由(1)的分析该反应为放热反应,则反应物总能量大于生成物总能量.
解答 解:(1)1mol H2和1mol I2充分反应生成2molHI,旧键断裂吸收能量的值为:436kJ+151kJ=587kJ,新键生成释放能量为:299kJ×2=598kJ,旧键断裂吸收的能量小于新键生成释放的能量,反应为放热反应,放出的热量为:598KJ-587kJ=11kJ,所以放出11kJ,
故答案为:587;598;放热反应;
(2)由(1)的分析该反应为放热反应,则反应物总能量大于生成物总能量,所以B正确;
故选:B.
点评 本题考查了焓变的计算及其与吸放热的图象分析,题目难度不大,注意旧键断裂吸收能量,新键生成释放能量.


科目:高中化学 来源: 题型:填空题
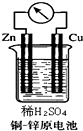 如图所示的铜-锌原电池中,理论上应观察到的现象是:
如图所示的铜-锌原电池中,理论上应观察到的现象是:查看答案和解析>>
科目:高中化学 来源: 题型:计算题
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 工业上合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g)△H<0.500℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示
工业上合成甲醇的反应为:CO(g)+2H2(g)?CH3OH(g)△H<0.500℃,5MPa条件下,将0.20mol CO与0.58mol H2的混合气体充入2L恒容密闭容器发生反应,反应过程中甲醇的物质的量浓度随时间的变化如图所示查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 .有机物X的键线式为
.有机物X的键线式为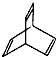
 .
.查看答案和解析>>
科目:高中化学 来源: 题型:解答题
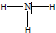 .
.查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com