下列溶液中溶质的物质的量浓度为1mol?L-1的是( )
A.将40gNaOH溶解于1L水中配成的NaOH溶液
B.常温常压下将22.4LHCl气体溶于水配成1L的盐酸溶液
C.将1L10mol/L的浓盐酸与9L水混合配成溶液
D.从1000mL1mol/LNaCl溶液中取出100mL的溶液
【答案】
分析:A、C=
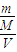
=
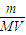
中,体积指溶液体积不是溶剂体积.
B、根据温度、压强对气体摩尔体积的影响分析判断.
C、根据不同液体混合时体积能否直接加和判断.
D、根据溶液浓度的均一性判断.
解答:解:A、C=
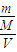
=
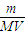
中,体积指溶液体积不是溶剂体积,所以40gNaOH溶解于1L水中配成的NaOH溶液浓度不是1mol/L,故A错误.
B、气体摩尔体积受温度和压强的影响,温度越高,气体摩尔体积越大,标况下,22.4LHCl的物质的量是1mol,常温常压下,22.4LHCl的物质的量小于1mol,所以常温常压下将22.4LHCl气体溶于水配成1L的盐酸溶液的物质的量浓度不是1mol/L,故B错误.
C、1L10mol/L的浓盐酸与9L水混合配成溶液的体积不是10L,所以混合后溶液的物质的量浓度不是1mol/L,故C错误.
D、溶液的物质的量浓度有均一性,与取出溶液的体积大小无关,故D正确.
故选D.
点评:本题考查了有关物质的量浓度的问题,难度不大,注意溶液的浓度有均一性,与取出溶液的体积大小无关.

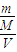 =
=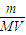 中,体积指溶液体积不是溶剂体积.
中,体积指溶液体积不是溶剂体积.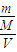 =
=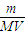 中,体积指溶液体积不是溶剂体积,所以40gNaOH溶解于1L水中配成的NaOH溶液浓度不是1mol/L,故A错误.
中,体积指溶液体积不是溶剂体积,所以40gNaOH溶解于1L水中配成的NaOH溶液浓度不是1mol/L,故A错误.
